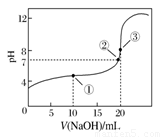
室温下,下列叙述正确的是(溶液体积变化忽略不计)
|
|
① |
② |
③ |
④ |
|
溶液 |
氨水 |
氢氧化钠溶液 |
醋酸 |
盐酸 |
|
pH |
11 |
11 |
3 |
3 |
A.在①、②中分别加入氯化铵晶体,两溶液的pH均增大
B.①、④两溶液等体积混合,所得溶液中c(C1-)>c(NH4+)>c(OH-)>c(H+)
C.②、③两溶液混合,若所得溶液的pH=7,则c(CH3COO-)>c(Na+)
D.分别将等体积的③和④加水稀释100倍,所得溶液的pH:③<④
下列说法正确的是:
A.已知某温度下纯水中的C(H+)=2×l0-7mol/L,据此无法求出水中C(OH-)
B.常温,Mg(OH)2能溶于氯化铵浓溶液主要原因是NH4+结合OH-使沉淀溶解平衡发生移动
C.已知:
|
共价键 |
C—C |
C=C |
C—H |
H—H |
|
键能/kJ·mol-1 |
348 |
610 |
413 |
436 |
上表数据可以计算出 (g)+3H2(g)→
(g)+3H2(g)→ (g)的焓变
(g)的焓变
D.已知MgCO3的KSP=6.82×l0-6,则在含有固体MgCO3的MgCl2、Na2CO3溶液中,都有c(Mg2+) =c(CO32-),且c(Mg2+)·c(CO32-) = 6.82×10-6 mol2/L2
(6分) 短周期元素X、Y、Z、M、N原子序数依次增大,有关信息如下:
|
元素 |
有关信息 |
|
X |
最外层电子数是次外层的2倍 |
|
Y |
元素主要化合价为-2价 |
|
Z |
其单质及化合物的焰色为黄色 |
|
M |
与X同主族,其单质为半导体材料 |
|
N |
其单质在Y单质中燃烧,发出明亮的蓝紫色火焰 |
XY2的电子式是 ;Z2Y2中所含化学键类型是 ;
XY2与Z2Y2反应的化学方程式是 。
(9分)下图是元素周期表的一部分,A、B、C、D、E、X是周期表给出元素组成的常见单质或化合物。
|
① |
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
④ |
⑤ |
⑥ |
|
|
||||||||||
|
② |
|
|
③ |
|
|
|
⑦ |
|
|||||||||
|
|
|
|
|
|
|
|
Fe |
|
|
|
|
|
|
|
|
|
|
I.已知A、B、C、D、E、X存在如图所示转化关系(部分生成物和反应条件略去)
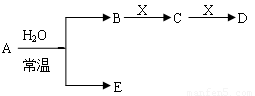
(1)若E为氧化物,则A与水反应的化学方程式为 ,①当X是碱性盐溶液,C分子中有22个电子时,表示X呈碱性的离子方程式为
②当X为金属单质时,则X与B的稀溶液反应生成C的离子反应方程式为
(2)若E为单质气体,D为白色沉淀,A的化学式可能是
 混合,所得溶液中一定存在:c (K+)+ c (H+) = c
(CH3COO-) + c (OH-)
混合,所得溶液中一定存在:c (K+)+ c (H+) = c
(CH3COO-) + c (OH-) H+ + OH-。下列叙述中,正确的是
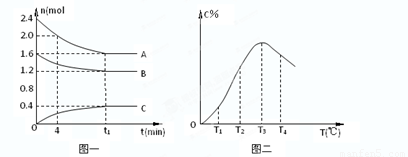
H+ + OH-。下列叙述中,正确的是  B(g)+C(s),达到化学平衡后,升高温度,容器内气体的密度增大,则下列叙述正确的是
B(g)+C(s),达到化学平衡后,升高温度,容器内气体的密度增大,则下列叙述正确的是