0 68078 68086 68092 68096 68102 68104 68108 68114 68116 68122 68128 68132 68134 68138 68144 68146 68152 68156 68158 68162 68164 68168 68170 68172 68173 68174 68176 68177 68178 68180 68182 68186 68188 68192 68194 68198 68204 68206 68212 68216 68218 68222 68228 68234 68236 68242 68246 68248 68254 68258 68264 68272 203614






 ,找出其中一个变化与“
,找出其中一个变化与“ ”组成一个反应,写出该反应的离子方程式____
。
”组成一个反应,写出该反应的离子方程式____
。
 由此可知,高锰酸根离子(MnO—4)反应后的产物与 有关。
由此可知,高锰酸根离子(MnO—4)反应后的产物与 有关。

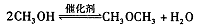
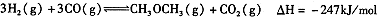
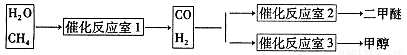
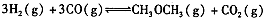 在密闭容器中达到平衡后,要提高CO的转化率,可以采取的措施是____。
在密闭容器中达到平衡后,要提高CO的转化率,可以采取的措施是____。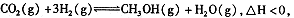 反应达到平衡时,改变温度(T)和压强(P),反应混合物CH3OH“物质的量分数”变化情况如图所示,关于温度(T)和压强(P)的关系判断正确的是 .(填序号)。
反应达到平衡时,改变温度(T)和压强(P),反应混合物CH3OH“物质的量分数”变化情况如图所示,关于温度(T)和压强(P)的关系判断正确的是 .(填序号)。 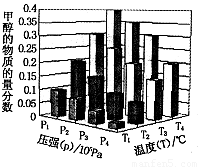
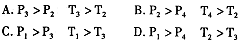
 写出平衡常数的表达式: 。如果温度降低,该反应的平衡常数 。(填“不变”、
写出平衡常数的表达式: 。如果温度降低,该反应的平衡常数 。(填“不变”、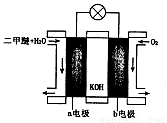



 。该反应在溶液中能发生的理由是:
。
。该反应在溶液中能发生的理由是:
。
