0 68059 68067 68073 68077 68083 68085 68089 68095 68097 68103 68109 68113 68115 68119 68125 68127 68133 68137 68139 68143 68145 68149 68151 68153 68154 68155 68157 68158 68159 68161 68163 68167 68169 68173 68175 68179 68185 68187 68193 68197 68199 68203 68209 68215 68217 68223 68227 68229 68235 68239 68245 68253 203614


 2Cl2+2H2O,可实现氯的循环利用。
2Cl2+2H2O,可实现氯的循环利用。

 +8H+=5Fe3++Mn2++4H2O),步骤为:
+8H+=5Fe3++Mn2++4H2O),步骤为:
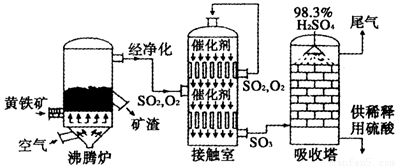
 Fe2O3+SO2↑+SO3↑+14H2O↑。利用下图装置可检验该反应的气体产物。
Fe2O3+SO2↑+SO3↑+14H2O↑。利用下图装置可检验该反应的气体产物。
 CH3OH(g)
CH3OH(g)