题目内容
已知在25℃时,FeS、CuS的溶度积常数(Ksp)分别为6.3×10-18、1.3×10-36。常温时下列有关说法正确的是
A.除去工业废水中的Cu2+可以选用FeS作沉淀剂
B.向H2S的饱和溶液中通入少量SO2气体溶液的酸性增强
C.因为H2SO4是强酸,所以反应:CuSO4十H2S=CuS↓+H2SO4不能发生
D.将足量的CuSO4溶解在0.1 mol/L的H2S溶液中,溶液中Cu2+的最大浓度为1.3×10-35mol/L
A
【解析】
试题分析:A、氯化铜的溶解度小于硫化亚铁的,根据沉淀容易向生成更难溶的方向进行可知,除去工业废水中的Cu2+可以选用FeS作沉淀剂,A正确;B、SO2具有氧化性,H2S具有还原性,二者混合发生氧化还原反应生成单质S和水,B不正确;C、由于硫化铜不溶于水,也不溶于硫酸中,所以反应CuSO4十H2S=CuS↓+H2SO4能发生,C不正确;H2S是弱电解质,在溶液中存在电离平衡。所以0.1 mol/L的H2S溶液中氢离子的浓度小于0.1mol/L,则将足量的CuSO4溶解在0.1 mol/L的H2S溶液中,溶液中Cu2+的最大浓度应该大于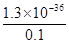 =1. 3×10-35mol/L,D不正确,答案选A。
=1. 3×10-35mol/L,D不正确,答案选A。
考点:考查溶度积常数的有关判断、应用和计算

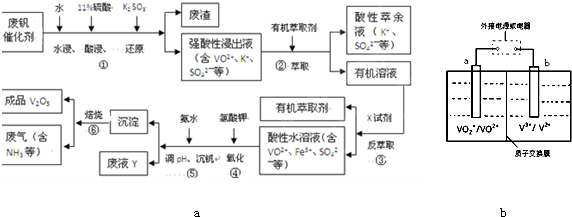
回答下列问题:
(1)①中废渣的主要成分是
(2)完成④中反应的离子方程式:
(3)25℃时,取样进行实验分析,得到钒沉淀率和溶液pH之间的关系如下表
| pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
| 钒沉淀率/% | 88.1 | 94.8 | 96.5 | 98.0 | 98.8 | 98.8 | 96.4 | 93.1 | 89.3 |
(4)全矾液流电池是一种新型电能储存和高效转化装置(如图b所示,a、b均为惰性电极),已知:全矾液流电池的工作原理为:
VO2++V2++2H+
| 放电 |
| 充电 |
V2+为紫色,V3+为绿色,VO2+为蓝色,VO2+为黄色.则:
①放电过程中,当转移1.0mol电子时共有1.0mol H+从
②当充电时,右槽溶液颜色由
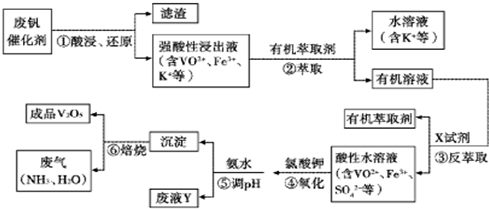
回答下列问题:
(1)①中滤渣的主要成分是
(2)②、③中的变化过程可简化为(下式中Rn+表示VO2+或Fe3+,HA表示有机萃取 剂的主要成分):
Rn+(水层)+nHA(有机层)?RAn(有机层)+nH+(水层)
②中萃取时必须加入适量碱,其原因是
(3)完成④中反应的离子方程式:
- 3 |
(4)25℃时,取样进行实验分析,得到钒沉淀率和溶液pH之间的关系如表
| pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
| 钡沉淀率/% | 88 | 92 | 93 | 95 | 95 | 95 | 93 | 90 | 87 |
(5)在整个工艺流程中,可以循环利用的物质是水、
(6)写出废液Y中除H+之外的两种阳离子
工业上设计将VOSO4中的K2SO4、SiO2杂质除去并回收得到V2O5的流程如下:
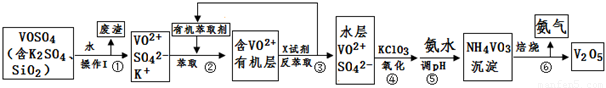
请回答下列问题:
(1)步骤①所得废渣的成分是 (写化学式),操作I的名称 。
(2)步骤②、③的变化过程可简化为(下式R表示VO2+,HA表示有机萃取剂):
R2(SO4)n (水层)+ 2nHA(有机层)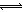 2RAn(有机层) + nH2SO4 (水层)
2RAn(有机层) + nH2SO4 (水层)
②中萃取时必须加入适量碱,其原因是 。
③中X试剂为 。
(3)⑤的离子方程式为 。
(4)25℃时,取样进行试验分析,得到钒沉淀率和溶液pH之间关系如下表:
|
pH |
1.3 |
1.4 |
1.5 |
1.6 |
1.7 |
1.8 |
1.9 |
2.0 |
2.1 |
|
钒沉淀率% |
88.1 |
94.8 |
96.5 |
98.0 |
98.8 |
98.8 |
96.4 |
93.1 |
89.3 |
结合上表,在实际生产中,⑤中加入氨水,调节溶液的最佳pH为 ;若钒沉淀率为93.1%时不产生Fe(OH)3沉淀,则溶液中c(Fe3+)< 。〖已知:25℃时,Ksp[Fe(OH)3]=2.6×10-39〗
(5)该工艺流程中,可以循环利用的物质有 和 。
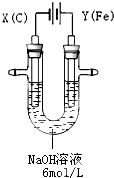 高铁酸钾(K2FeO4)具有高效的消毒作用,为一种新型非氯高效消毒剂.电解法制备高铁酸钾操作简便,成功率高,易于实验室制备.其原理如图所示.
高铁酸钾(K2FeO4)具有高效的消毒作用,为一种新型非氯高效消毒剂.电解法制备高铁酸钾操作简便,成功率高,易于实验室制备.其原理如图所示.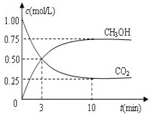 2009年10月15日新华社报道:全国农村应当在“绿色生态-美丽多彩-低碳节能-循环发展”的理念引导下,更快更好地发展“中国绿色村庄”,参与“亚太国际低碳农庄”建设.可见“低碳循环”已经引起了国民的重视,试回答下列问题:
2009年10月15日新华社报道:全国农村应当在“绿色生态-美丽多彩-低碳节能-循环发展”的理念引导下,更快更好地发展“中国绿色村庄”,参与“亚太国际低碳农庄”建设.可见“低碳循环”已经引起了国民的重视,试回答下列问题: