某同学进行试验探究时,欲配制1.0molL-1Ba(OH)2溶液,但只找到在空气中暴露已久的Ba(OH)2·8H2O试剂(化学式量:315)。在室温下配制溶液时发现所取试剂在水中仅部分溶解,烧杯中存在大量未溶物。
为探究原因,该同学查得Ba(OH)2·8H2O 部分溶解度数据,见下表:
|
温度 |
283K |
293K |
303K |
|
溶解度(g/100g H2O) |
2.5 |
3.9 |
5.6 |
(1)烧杯中未溶物仅为BaCO3,理由是 。
(2)假设试剂由大量Ba(OH)2·8H2O和少量BaCO3组成,设计试验方案,进行成分检验,在答题纸上写出实验步骤、预期现象和结论。(不考虑结晶水的检验;室温时BaCO3饱和溶液的pH=9.6)
限选试剂及仪器:稀盐酸、稀硫酸、NaOH溶液、澄清石灰水、pH计、烧杯、试管、带塞导气管、滴管
|
实验步骤 |
预期现象和结论 |
|
步骤1:取适量试剂于洁净烧杯中,加入足量蒸馏水,充分搅拌,静置,过滤,得滤液和沉淀。 |
###### |
|
步骤2:取适量滤液于试管中,滴加稀硫酸。 |
_______________________ |
|
步骤3:取适量步骤1中的沉淀于试管中, ,连接带塞导气管将产生的气体导入澄清石灰水中。 |
_______________________ ______________________ |
|
步骤4:取步骤1中的滤液于烧杯中,______________________________ |
_______________________,说明该试剂中含有Ba(OH)2。 |
(3)将试剂初步提纯后,准确测定其中Ba(OH)2·8H2O的含量。
实验如下:①配制250 mL 约0.1mol·L-1Ba(OH)2·8H2O溶液:准确称取w克试样,置于烧杯中,加适量蒸馏水,搅拌,将溶液转入 ,洗涤,定容,摇匀.
②滴定:准确量取25.00ml所配制Ba(OH)2溶液于锥形瓶中,滴加指示剂,将 (填“0.020”、“0.05”、“0.1980”或“1.5”)molL-1盐酸装入50ml酸式滴定管,滴定至终点,记录数据。重复滴定2次。平均消耗盐酸Vml。
(4)室温下, (填“能”或“不能”) 配制1.0 mol·L-1Ba(OH)2溶液,说明理由________________________________________________________________________________________.
 )是组成人体蛋白质的氨基酸之一,它可由A通过以下反应合成制取。有机物A(
)是组成人体蛋白质的氨基酸之一,它可由A通过以下反应合成制取。有机物A( )为食品包装中的常用防腐剂,常温下难溶于水, 可以使溴水褪色。有机物B(
)为食品包装中的常用防腐剂,常温下难溶于水, 可以使溴水褪色。有机物B( ),其分子中没有支链,通常状况下为无色晶体,能与氢氧化钠溶液发生反应。
),其分子中没有支链,通常状况下为无色晶体,能与氢氧化钠溶液发生反应。


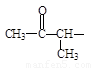 、且属于酯类的同分异构
、且属于酯类的同分异构 。,
。, )也可以发生“Diels-Alder反应”,该化学反应方程式为:
)也可以发生“Diels-Alder反应”,该化学反应方程式为: