用图示装置制取PCl3,在E中放入足量白磷,将氯气不间断地通入E,氯气与白磷就会发生反应,并放出热量(温度高于75℃).已知:PCl3和PCl5遇水强烈反应,它们熔沸点数据如下:

请根据图中装置回答下列问题:
(1)检查该装置气密性的方法是 .
(2)为得到氯气,若B中加入MnO2,则A中应加入 ,发生反应的化学方程式为 .
(3)若发现C中气泡产生过猛,需要进行的操作的关键是 .
(4)在反应开始时主要生成PCl3,而后来主要生成PCl5,原因可能是 ;从PCl3和PCl5的混合物中分离也PCl3的最佳方法是 (选填序号).
a.蒸馏b.分液c.升华
(5)生成的PCl3在G中收集,则F中盛有 ,作用是
(6)C、D、H所盛的试剂分别是:C ;D ;H .
(7)如果E中反应放热较多,G处的导管可能发生堵塞,其原因是 .

| 熔点 | 沸点 | |
| PCl3 | -112℃ | 75℃ |
| PCl5 | 148℃ | 200℃ |
(1)检查该装置气密性的方法是 .
(2)为得到氯气,若B中加入MnO2,则A中应加入 ,发生反应的化学方程式为 .
(3)若发现C中气泡产生过猛,需要进行的操作的关键是 .
(4)在反应开始时主要生成PCl3,而后来主要生成PCl5,原因可能是 ;从PCl3和PCl5的混合物中分离也PCl3的最佳方法是 (选填序号).
a.蒸馏b.分液c.升华
(5)生成的PCl3在G中收集,则F中盛有 ,作用是
(6)C、D、H所盛的试剂分别是:C ;D ;H .
(7)如果E中反应放热较多,G处的导管可能发生堵塞,其原因是 .
已知25℃时部分弱电解质的电离平衡常数数据如下表:
回答下列问题:
(1)物质的量浓度均为0.1mol?L-1的四种溶液:a.CH3COOH b.Na2CO3 c.NaClO d.NaHCO3;pH由小到大的排列顺序是 (用字母表示)
(2)常温下,0.1mol?L-1的CH3COOH溶液加稀释过程中,下列表达式的数据变大的是
A.c(H+)B.c(H+)/c(CH3COOH)
C.c(H+)?c(OH-)D.c(OH-)/c(H+)
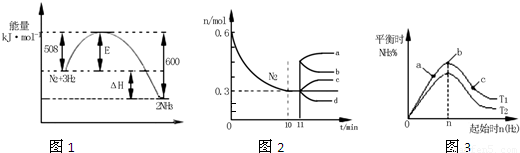
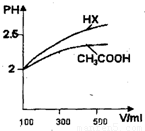
(3)体积均为100mL pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则HX的电离平衡常数 CH3COOH的电离平衡常数(填大于、小于或等于)理由是
(4)25℃时,CH3COOH与CH3COONa的混合溶液,若测得pH=6,则溶液中c(CH3COO-)-c(Na+)= mol?L-1(填精确值),c(CH3COO-)/c(CH3COOH)= .
0 67774 67782 67788 67792 67798 67800 67804 67810 67812 67818 67824 67828 67830 67834 67840 67842 67848 67852 67854 67858 67860 67864 67866 67868 67869 67870 67872 67873 67874 67876 67878 67882 67884 67888 67890 67894 67900 67902 67908 67912 67914 67918 67924 67930 67932 67938 67942 67944 67950 67954 67960 67968 203614
| 化学式 | CH3COOH | H2CO3 | HClO | |
| 平衡常数 | Ka=1.8×10-5 | Ka1=4.3×10-7 | Ka2=5.6×10-11 | Ka=3.0×10-4 |
(1)物质的量浓度均为0.1mol?L-1的四种溶液:a.CH3COOH b.Na2CO3 c.NaClO d.NaHCO3;pH由小到大的排列顺序是 (用字母表示)
(2)常温下,0.1mol?L-1的CH3COOH溶液加稀释过程中,下列表达式的数据变大的是
A.c(H+)B.c(H+)/c(CH3COOH)
C.c(H+)?c(OH-)D.c(OH-)/c(H+)
(3)体积均为100mL pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则HX的电离平衡常数 CH3COOH的电离平衡常数(填大于、小于或等于)理由是
(4)25℃时,CH3COOH与CH3COONa的混合溶液,若测得pH=6,则溶液中c(CH3COO-)-c(Na+)= mol?L-1(填精确值),c(CH3COO-)/c(CH3COOH)= .