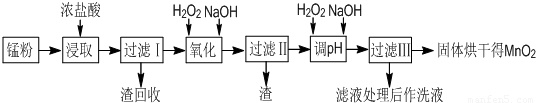
某混合粉末一定有Al2O3可能有ZnO中的一种或几种物质,请设计合理实验探究该混合物中Fe2O3、ZnO的存在﹛提示:Zn(OH)2类似Al(OH)3也是两性物质,溶于烧碱溶液生成Na2ZnO2;且Zn(OH)2溶于浓NH3水生成[Zn(NH3)4](OH)2而Al(OH)3不溶于浓NH3水.限选择的仪器和试剂:
烧杯、试管、玻璃棒、酒精灯、漏斗、过滤架、滤纸、量筒、容量瓶、滴管、药匙;1mol/L硫酸、2mol/L硝酸、2mol/LNaOH溶液、10%KSCN溶液、稀氨水.
完成以下实验探究过程:
(1)提出假设:
假设1 该混合物中除Al2O3外还含有______;
假设2 该混合物中除Al2O3外还含有______;
假设3 该混合物中除Al2O3外还含有Fe2O3、ZnO.
(2)设计实验方案:基于假设3,设计出实验方案.请在下表对应栏目叙述实验操作、预期现象和结论(实验步骤可以不填满、也可以增加):
烧杯、试管、玻璃棒、酒精灯、漏斗、过滤架、滤纸、量筒、容量瓶、滴管、药匙;1mol/L硫酸、2mol/L硝酸、2mol/LNaOH溶液、10%KSCN溶液、稀氨水.
完成以下实验探究过程:
(1)提出假设:
假设1 该混合物中除Al2O3外还含有______;
假设2 该混合物中除Al2O3外还含有______;
假设3 该混合物中除Al2O3外还含有Fe2O3、ZnO.
(2)设计实验方案:基于假设3,设计出实验方案.请在下表对应栏目叙述实验操作、预期现象和结论(实验步骤可以不填满、也可以增加):
| 实验步聚 | 实验操作 | 预期现象和结论 |
| 第一步 | ______ | ______ |
| 第二步 | ______ | ______ |
| 第三步 | ______ | ______ |
| 第四步 | ______ | ______ |
硫酸的消费量常被作为国家工业发展水平的一种标志.工业合成硫酸最重要一步:2SO2(g)+O2 (g)?2SO3(g)△H<0.在一定条件下,将2mol SO2(g) 和1mol O2 (g) 充入2L密闭容器中,反应从起始到平衡后压强变为原来的11/15.回答下列问题:
(1)下表为2SO2(g)+O2 (g)?2SO3(g)反应的温度和压强对SO2转化率的影响:
你认为最好选择的压强是______理由是:______.
(2)请计算题干条件下SO2的平衡转化率及SO3(g)?SO2(g)+1/2O2 (g)的平衡常数,写出计算过程(最后一步不必算出精确数值):
(1)下表为2SO2(g)+O2 (g)?2SO3(g)反应的温度和压强对SO2转化率的影响:
| 压强/MPa 温度/℃ | 0.1 | 0.5 | 1 | 10 | 常压为1.01x105 =101kPa =0.1MPa |
| 400 | 99.2% | 99.6% | 99.7% | 99.9% | |
| 500 | 93.5% | 96.9% | 97.8% | 98.7% | |
| 600 | 73.7% | 85.8% | 89.5% | 96.4% |
(2)请计算题干条件下SO2的平衡转化率及SO3(g)?SO2(g)+1/2O2 (g)的平衡常数,写出计算过程(最后一步不必算出精确数值):
用如图装置进行实验,请回答下列问题:
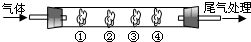
I.(1)若通入SO2气体,请填写表中空格:
(2)写出③中反应的离子方程式:______
II.若通入HCl气体,装置中的四处棉花依次做了如下处理:①包有用水润湿某固体物质、②浸有KI溶液、③浸有石蕊溶液、④浸有浓NaOH溶液.请回答:
(1)观察到②处棕黄色物质产生,则:①处包有的某固体物质可能是下列的______(填下面物质的序号),其反应的离子方程式为______.
a.MnO2 b.KMnO4 c.KCl d.Cu
(2)在实验过程中,在③处能观察到______.
(3)反应较长时间后,②处棕黄色褪去,生成无色的IO3-,该反应的离子方程式为______.
0 67658 67666 67672 67676 67682 67684 67688 67694 67696 67702 67708 67712 67714 67718 67724 67726 67732 67736 67738 67742 67744 67748 67750 67752 67753 67754 67756 67757 67758 67760 67762 67766 67768 67772 67774 67778 67784 67786 67792 67796 67798 67802 67808 67814 67816 67822 67826 67828 67834 67838 67844 67852 203614

I.(1)若通入SO2气体,请填写表中空格:
| B中棉花的位置 | ① | ② | ③ | ④ |
| 棉花浸取试剂 | 石蕊试液 | 品红溶液 | 淀粉和碘水混合液 | 氢硫酸 |
| 现象 | ______ | ______ | 褪色 | 浅黄色 |
| 体现SO2的性质 | 水溶液显酸性 | 漂白性 | ______ | 氧化性 |
II.若通入HCl气体,装置中的四处棉花依次做了如下处理:①包有用水润湿某固体物质、②浸有KI溶液、③浸有石蕊溶液、④浸有浓NaOH溶液.请回答:
(1)观察到②处棕黄色物质产生,则:①处包有的某固体物质可能是下列的______(填下面物质的序号),其反应的离子方程式为______.
a.MnO2 b.KMnO4 c.KCl d.Cu
(2)在实验过程中,在③处能观察到______.
(3)反应较长时间后,②处棕黄色褪去,生成无色的IO3-,该反应的离子方程式为______.
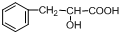
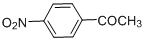 的同分异构体很多,其含有-NO2、-CHO、-CH3、
的同分异构体很多,其含有-NO2、-CHO、-CH3、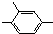 四种基团的同分异构体有多种,其中至少有2个取代基处于苯环对位的同分异构体有6种,它们的结构简式为:
四种基团的同分异构体有多种,其中至少有2个取代基处于苯环对位的同分异构体有6种,它们的结构简式为: 、
、 、
、 、
、 ______、______.
______、______.
 Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-