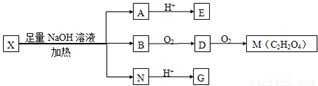
下表各组物质之间通过一步反应就能实现如 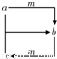 所示转化的是( )
所示转化的是( )
A.A
B.B
C.C
D.D
 所示转化的是( )
所示转化的是( )| 物质选项 | a | b | c | m |
| A | N2 | NO | HNO3 | O2 |
| B | Cl2 | FeCl3 | FeCl2 | Fe |
| C | Na2CO3 | NaHCO3 | NaOH | CO2 |
| D | CH3CH2OH | CH3CHO | CH3COOH | O2 |
A.A
B.B
C.C
D.D
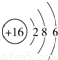
有四种短周期元素,它们的结构、性质等信息如下表所述:
请根据表中信息填写:
(1)X元素在周期表中的位置 ;其气态氢化物的电子式 ;
(2)工业上制取Y单质常用的方法是 ;
(3)Y离子半径比Z离子的半径 (填“小”或“大”);
(4)Z的单质和氧化铁反应可用于野外焊接钢轨,写出反应的化学方程式 ;
(5)Z的某种盐是常用的净水剂,用离子方程式表示其净水原理 ;
(6)举出实例说明M的非金属性比X强(用化学方程式表示) .
| 元素 | 结构、性质等信息 |
| X | 构成有机物的主角,该元素的一种氧化物和气态氢化物都是典型的温室气体. |
| Y | 短周期中(除稀有气体外)原子半径最大的元素,该单质液态时可用作核反应堆的传热介质. |
| Z | 与Y同周期,其最高价氧化物的水化物呈两性. |
| M | 海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂. |
(1)X元素在周期表中的位置 ;其气态氢化物的电子式 ;
(2)工业上制取Y单质常用的方法是 ;
(3)Y离子半径比Z离子的半径 (填“小”或“大”);
(4)Z的单质和氧化铁反应可用于野外焊接钢轨,写出反应的化学方程式 ;
(5)Z的某种盐是常用的净水剂,用离子方程式表示其净水原理 ;
(6)举出实例说明M的非金属性比X强(用化学方程式表示) .
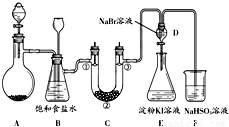
某课外小组同学用如图所示装置在实验室制备氯气并探究其相关性质(夹持设备已略).
(1)制备氯气选用的药品为:漂粉精固体和浓盐酸,相关的离子反应方程式为:
;
(2)装置B的作用之一是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象 ;
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中①、②、③依次放入 ;(选填字母)
(4)设计装置D、E的目的是比较氯、溴、碘的非金属性.当向D中缓缓通入一定量氯气时,可以看到无色溶液逐渐变为 色,说明氯的非金属性大于溴;之后打开活塞,将装置D中少量溶液加入装置E中,振荡;观察到的现象是 ,则说明溴的非金属性大于碘;
(5)有同学提出该实验方案仍有不足,请说明其中两点不足及原因是:① ;② .
0 67606 67614 67620 67624 67630 67632 67636 67642 67644 67650 67656 67660 67662 67666 67672 67674 67680 67684 67686 67690 67692 67696 67698 67700 67701 67702 67704 67705 67706 67708 67710 67714 67716 67720 67722 67726 67732 67734 67740 67744 67746 67750 67756 67762 67764 67770 67774 67776 67782 67786 67792 67800 203614
(1)制备氯气选用的药品为:漂粉精固体和浓盐酸,相关的离子反应方程式为:
;
(2)装置B的作用之一是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象 ;
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中①、②、③依次放入 ;(选填字母)
| ① | ② | ③ | |
| a | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
| b | 干燥的有色布条 | 硅 胶 | 湿润的有色布条 |
| c | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
| d | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
(5)有同学提出该实验方案仍有不足,请说明其中两点不足及原因是:① ;② .

 I
I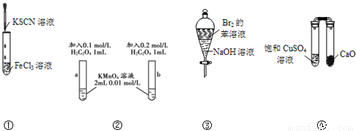
 +Ba2++2OH-=BaCO3↓+2H2O
+Ba2++2OH-=BaCO3↓+2H2O 2Cu+2H2↑+O2↑
2Cu+2H2↑+O2↑
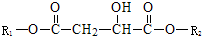 (其中R1、R2为未知部分的结构;R2中含有Br原子),为推测X的分子结构,进行如图的转化:
(其中R1、R2为未知部分的结构;R2中含有Br原子),为推测X的分子结构,进行如图的转化: