在800℃时,在2L密闭容器中将一定量的NO和O2混合发生反应2NO+O2?2NO2,n(NO)随时间的变化如下表:
请回答下列问题:
(1)用O2表示从0~20s内该反应的速率为 ;达到平衡时NO的转化率为 .
(2)若升温到850℃,平衡后n(NO)=n(NO2),则该反应是 热反应(填:“吸”、“放”)
(3)下列能说明该反应已达到平衡的是 .
A.容器内压强不变 B.容器内气体密度不变
C.n(NO)=n(NO2) D.容器内气体颜色不变
E.容器内混合气体的平均分子量不变 F.v(NO2)=2v(O2)
(4)若改变某一条件,达新平衡时n(NO)=0.06mol,下列说法正确的是 .
A.平衡一定正向移动
B.可能是向容器中加入了一定量的NO气体
C.NO的转化率一定增大
D.可能是缩小了容器的体积
(5)假设在一定条件下0.2molNO气体与氧气反应,达到平衡时测得放出热量akJ,此时NO转化率为80%,写出在此条件下该反应的热化学方程式 .
0 67582 67590 67596 67600 67606 67608 67612 67618 67620 67626 67632 67636 67638 67642 67648 67650 67656 67660 67662 67666 67668 67672 67674 67676 67677 67678 67680 67681 67682 67684 67686 67690 67692 67696 67698 67702 67708 67710 67716 67720 67722 67726 67732 67738 67740 67746 67750 67752 67758 67762 67768 67776 203614
| 时间/s | 10 | 20 | 30 | 40 | 50 | |
| n(NO)/mol | 0.2 | 0.1 | 0.08 | 0.07 | 0.07 | 0.07 |
(1)用O2表示从0~20s内该反应的速率为 ;达到平衡时NO的转化率为 .
(2)若升温到850℃,平衡后n(NO)=n(NO2),则该反应是 热反应(填:“吸”、“放”)
(3)下列能说明该反应已达到平衡的是 .
A.容器内压强不变 B.容器内气体密度不变
C.n(NO)=n(NO2) D.容器内气体颜色不变
E.容器内混合气体的平均分子量不变 F.v(NO2)=2v(O2)
(4)若改变某一条件,达新平衡时n(NO)=0.06mol,下列说法正确的是 .
A.平衡一定正向移动
B.可能是向容器中加入了一定量的NO气体
C.NO的转化率一定增大
D.可能是缩小了容器的体积
(5)假设在一定条件下0.2molNO气体与氧气反应,达到平衡时测得放出热量akJ,此时NO转化率为80%,写出在此条件下该反应的热化学方程式 .
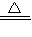 HCOO-+NH4++2Ag↓+H2O+3NH3
HCOO-+NH4++2Ag↓+H2O+3NH3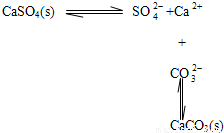
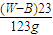
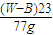
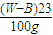
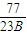 )g
)g