氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用.请回答下列问题:
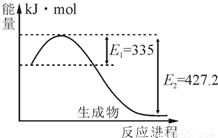
(1)如图是N2和H2反应生成2molNH3过程中能量变化示意图,请计算每生成1molNH3放出热量为 .
(2)工业合成氨气需要的反应条件非常高且产量低,而一些科学家采用高质子导电性的SCY陶瓷(能传递HH+)实现氨的电化学合成,从而大大提高了氮气和氢气的转化率.电化学合成氨过程的总反应式为:N2+3H2 2NH3,则在电化学合成氨的过程中,阴极反应式为 .
2NH3,则在电化学合成氨的过程中,阴极反应式为 .
(3)在固定体积的密闭容器中,进行如下化学反应:N2(g)+3H2(g)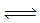 2NH3(g),△H<0,其化学平衡常数K与t的关系如下表:、C(H2)、C(NH3)分别为平衡浓度)
2NH3(g),△H<0,其化学平衡常数K与t的关系如下表:、C(H2)、C(NH3)分别为平衡浓度)
请完成下列问题:
①试确定K1的相对大小,K1 4.1×106(填写“>”“=”或“<”)
②下列各项能作为判断该反应达到化学平衡状态的依据的是 (填序号字母).
A.容器内N2、H2、NH3的浓度之比为1:3:2 B.2v(N2)(正)=v(H2)(逆)
C.容器内压强保持不变 D.混合气体的密度保持不变
(4)①NH4Cl溶液呈酸性,这是由于NH4+水解的缘故.则NH4Cl溶于重水(D2O)生成一水合氨和水合氢离子的化学式是 .
②某氨水的pH=x,某盐酸的pH=y,x+y=14,且x>11,将上述氨水和盐酸等体积混合后,所得溶液中各种离子的浓度由大到小的顺序为
A.C(Cl-)>C(NH4+)>C(H+)>C(OH-)
B.C(NH4+)>C(Cl-)>C(OH-)>C(H+)
C.C(Cl-)>C(NH4+)>C(OH-)>C(H+)
D.C(NH4+)>C(Cl-)>C(H+)>C(OH-)

(1)如图是N2和H2反应生成2molNH3过程中能量变化示意图,请计算每生成1molNH3放出热量为 .
(2)工业合成氨气需要的反应条件非常高且产量低,而一些科学家采用高质子导电性的SCY陶瓷(能传递HH+)实现氨的电化学合成,从而大大提高了氮气和氢气的转化率.电化学合成氨过程的总反应式为:N2+3H2
 2NH3,则在电化学合成氨的过程中,阴极反应式为 .
2NH3,则在电化学合成氨的过程中,阴极反应式为 .(3)在固定体积的密闭容器中,进行如下化学反应:N2(g)+3H2(g)
 2NH3(g),△H<0,其化学平衡常数K与t的关系如下表:、C(H2)、C(NH3)分别为平衡浓度)
2NH3(g),△H<0,其化学平衡常数K与t的关系如下表:、C(H2)、C(NH3)分别为平衡浓度)| t/K | 298 | 398 | 498 | … |
| K/-2 | 4.1×106 | K1 | K2 | … |
①试确定K1的相对大小,K1 4.1×106(填写“>”“=”或“<”)
②下列各项能作为判断该反应达到化学平衡状态的依据的是 (填序号字母).
A.容器内N2、H2、NH3的浓度之比为1:3:2 B.2v(N2)(正)=v(H2)(逆)
C.容器内压强保持不变 D.混合气体的密度保持不变
(4)①NH4Cl溶液呈酸性,这是由于NH4+水解的缘故.则NH4Cl溶于重水(D2O)生成一水合氨和水合氢离子的化学式是 .
②某氨水的pH=x,某盐酸的pH=y,x+y=14,且x>11,将上述氨水和盐酸等体积混合后,所得溶液中各种离子的浓度由大到小的顺序为
A.C(Cl-)>C(NH4+)>C(H+)>C(OH-)
B.C(NH4+)>C(Cl-)>C(OH-)>C(H+)
C.C(Cl-)>C(NH4+)>C(OH-)>C(H+)
D.C(NH4+)>C(Cl-)>C(H+)>C(OH-)
某校研究性学习小组对过量炭粉与氧化铁反应产物中气体的成分进行研究.

(1)提出假设:该反应的气体产物全部是二氧化碳.
(2)设计方案:将一定量的氧化铁在隔绝氧气条件下与过量炭粉完全反应(如图),测定参加反应的碳元素与氧元素的质量比.
(3)查阅资料:氮气不与炭粉、氧化铁发生反应,可用来隔绝氧气.实验室可以用氯化铵饱和溶液和亚硝酸钠饱和溶液混合加热反应制得氮气.请写出该反应的离子方程式: .
(4)实验操作:
(5)数据处理:经计算,参加反应的碳元素质量为 g.
(6)得到结论:根据数据处理结果,得出原假设不成立,理由是:
(7)根据数据处理结果,反应生成的气体是 ,该实验的化学方程式为: .
(8)该实验设计存在不合理之处,请指出并说明改进方法 .
0 67535 67543 67549 67553 67559 67561 67565 67571 67573 67579 67585 67589 67591 67595 67601 67603 67609 67613 67615 67619 67621 67625 67627 67629 67630 67631 67633 67634 67635 67637 67639 67643 67645 67649 67651 67655 67661 67663 67669 67673 67675 67679 67685 67691 67693 67699 67703 67705 67711 67715 67721 67729 203614

(1)提出假设:该反应的气体产物全部是二氧化碳.
(2)设计方案:将一定量的氧化铁在隔绝氧气条件下与过量炭粉完全反应(如图),测定参加反应的碳元素与氧元素的质量比.
(3)查阅资料:氮气不与炭粉、氧化铁发生反应,可用来隔绝氧气.实验室可以用氯化铵饱和溶液和亚硝酸钠饱和溶液混合加热反应制得氮气.请写出该反应的离子方程式: .
(4)实验操作:
| 操作步骤及实验现象 | 简答 |
| ①称取3.2g氧化铁与2g炭粉均匀混合,放入48.48g的玻璃管中,按如图装置连接 | |
| ②加热前,先通一段时间纯净、干燥的氮气 | 其目的是: |
| ③夹紧T处弹簧夹,加热一段时间,澄清石灰水变浑浊 | 该现象说明: |
| ④完全反应后,冷却至室温,称得玻璃管和固体的总质量为52.24g |
(6)得到结论:根据数据处理结果,得出原假设不成立,理由是:
(7)根据数据处理结果,反应生成的气体是 ,该实验的化学方程式为: .
(8)该实验设计存在不合理之处,请指出并说明改进方法 .








