下列有关物质检验的实验结论正确的是( )
A.A
B.B
C.C
D.D
| 选项 | 实验操作及现象 | 实验结论 |
| A | 向某溶液中加入盐酸酸化的氯化钡溶液,有白色沉淀生成 | 该溶液中一定含有SO42- |
| B | 向某溶液中加入2滴KSCN溶液,溶液不显红色.再向溶液中加入几滴新制的氯水,溶液变为红色 | 该溶液中一定含有Fe2+ |
| C | 某气体能使湿润的红色石蕊试纸变蓝 | 该气体水溶液一定显碱性 |
| D | 将少量某物质的溶液滴加到新制的银溶液中,水浴加热后有银镜生成 | 该物质一定属于醛类 |
A.A
B.B
C.C
D.D
某探究小组通过比较酸性KMnO4溶液与H2C2O4溶液反应过程中,溶液紫色消失时间长短的方法,研究浓度、温度对反应速率的影响.
可供选择的实验条件:KMnO4酸性溶液的浓度可选择0.01mol?L-1、0.1mol?L-1,H2C2O4溶液的浓度可选择0.1mol?L-1、0.2mol?L-1,实验温度可选择298K、323K.每次实验KMnO4酸性溶液的用量均为4mL、H2C2O4溶液的用量均为2mL.
(1)实验设计:请完成以下实验设计表.
(2)实验准备:配制上述溶液需要用到的玻璃仪器有 .
(3)实验过程:实验时控制温度为323K的方法是 .
(4)实验记录:实验中需要记录的数据是 .
可供选择的实验条件:KMnO4酸性溶液的浓度可选择0.01mol?L-1、0.1mol?L-1,H2C2O4溶液的浓度可选择0.1mol?L-1、0.2mol?L-1,实验温度可选择298K、323K.每次实验KMnO4酸性溶液的用量均为4mL、H2C2O4溶液的用量均为2mL.
(1)实验设计:请完成以下实验设计表.
| 实验编号 | T/K | KMnO4浓度 /mol?L-1 | H2C2O4浓度 /mol?L-1 | 实验目的 |
| ① | 298 | 0.01mol?L-1 | 0.1mol?L-1 | 为以下实验做对照 |
| ② | ||||
| ③ | 探究浓度对反应速率的影响 |
(3)实验过程:实验时控制温度为323K的方法是 .
(4)实验记录:实验中需要记录的数据是 .
某课外研究小组利用粗制氧化铜(含有少量铜)制取胆矾.他们设计了如下两种不同的制备途径:

(1)途径1中会产生一种污染环境的气体,该气体的化学式是 .
(2)写出途径2中所有反应的化学方程式 ;
(3)金属铜制品长期放置在潮湿的空气中,表面出现一层绿色物质,有关的化学方程式是 .
(4)下表中,对陈述Ⅰ、Ⅱ的正确性及其有无因果关系的判断都正确的是 (填字母).
0 67496 67504 67510 67514 67520 67522 67526 67532 67534 67540 67546 67550 67552 67556 67562 67564 67570 67574 67576 67580 67582 67586 67588 67590 67591 67592 67594 67595 67596 67598 67600 67604 67606 67610 67612 67616 67622 67624 67630 67634 67636 67640 67646 67652 67654 67660 67664 67666 67672 67676 67682 67690 203614

(1)途径1中会产生一种污染环境的气体,该气体的化学式是 .
(2)写出途径2中所有反应的化学方程式 ;
(3)金属铜制品长期放置在潮湿的空气中,表面出现一层绿色物质,有关的化学方程式是 .
(4)下表中,对陈述Ⅰ、Ⅱ的正确性及其有无因果关系的判断都正确的是 (填字母).
| 选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
| A | 青铜是我国使用最早的合金 | 合金是指多种金属熔合成的金属材料 | Ⅰ错;Ⅱ对;无 |
| B | 精炼铜时,粗铜板作阳极 | 铜具有良好的导电性 | Ⅰ对;Ⅱ对;无 |
| C | 铜锌原电池中,铜是正极 | CuO和Cu2O都是黑色固体 | Ⅰ错;Ⅱ错;无 |
| D | CuO能与水反应生成Cu(OH)2 | 金属氧化物都能与水反应生成相应的金属氢氧化物 | Ⅰ对;Ⅱ对;有 |
 LiNiO2
LiNiO2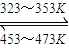 Ni(CO)4(g)
Ni(CO)4(g)
 出发来合成M,其合成路线如下:
出发来合成M,其合成路线如下:
