有关元素X、Y、Z、W的信息如下:
请回答下列问题:
(1)W的单质与Y的最高价氧化物对应的水化物反应的离子方程式为______
(2)铜片、碳棒和ZX3溶液组成原电池,写出正极发生的电极反应方程式______
(3)向淀粉碘化钾溶液中滴加几滴ZX3的浓溶液,现象为______,w3+离子的结构示意图______.
(4)以上述所得WX3溶液为原料制取无水WX3,先制得WX3?6H2O晶体,主要操作包括______,在______条件下加热WX3?6H2O晶体,能进一步制取无水WX3,其原因是(结合离子方程式简要说明)______.
| 元素 | 信息 |
| X | 所在主族序数与所在周期序数之差为4 |
| Y | 最高价氧化物对应的水化物,能电离出电子数相等的阴、阳离子 |
| Z | 单质是生活中常见金属,其制品在潮湿空气中易被腐蚀或损坏 |
| W | 该元素能形成两性氢氧化物 |
(1)W的单质与Y的最高价氧化物对应的水化物反应的离子方程式为______
(2)铜片、碳棒和ZX3溶液组成原电池,写出正极发生的电极反应方程式______
(3)向淀粉碘化钾溶液中滴加几滴ZX3的浓溶液,现象为______,w3+离子的结构示意图______.
(4)以上述所得WX3溶液为原料制取无水WX3,先制得WX3?6H2O晶体,主要操作包括______,在______条件下加热WX3?6H2O晶体,能进一步制取无水WX3,其原因是(结合离子方程式简要说明)______.
某工厂生产硼砂过程中产生的固体废料,主要含有MgCO3、MgSiO3、CaMg(CO3)2、Al2O3和Fe2O3等,回收其中镁的工艺流程如下:
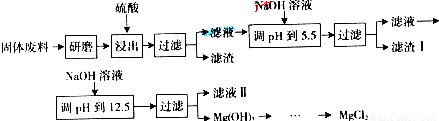
部分阳离子以氢氧化物形式完全深沉时溶液的pH由见上表,请回答下列问题:
(1)“浸出”步骤中,为提高镁的浸出率,可采取的措施有______(要求写出两条).
(2)滤渣I的主要成分有______.
(3)从滤液Ⅱ中可回收利用的主要物质有______.
(4)Mg(ClO3)2在农业上可用作脱叶剂、催熟剂,可采用复分解反应制备:
MgCl2+2NaClO3═Mg(ClO3)2+2NaCl
已知四种化合物的溶解度(S)随温度(T)变化曲线如下图所示:
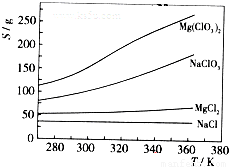
①将反应物按化学反应方程式计量数比混合制备Mg(ClO3)2.简述可制备Mg(ClO3)2的原因:______.
②按①中条件进行制备实验.在冷却降温析出Mg(ClO3)2过程中,常伴有NaCl析出,原因是:______.除去产品中该杂质的方法是:______.

| 沉淀物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| PH | 3.2 | 5.2 | 12.4 |
(1)“浸出”步骤中,为提高镁的浸出率,可采取的措施有______(要求写出两条).
(2)滤渣I的主要成分有______.
(3)从滤液Ⅱ中可回收利用的主要物质有______.
(4)Mg(ClO3)2在农业上可用作脱叶剂、催熟剂,可采用复分解反应制备:
MgCl2+2NaClO3═Mg(ClO3)2+2NaCl
已知四种化合物的溶解度(S)随温度(T)变化曲线如下图所示:

①将反应物按化学反应方程式计量数比混合制备Mg(ClO3)2.简述可制备Mg(ClO3)2的原因:______.
②按①中条件进行制备实验.在冷却降温析出Mg(ClO3)2过程中,常伴有NaCl析出,原因是:______.除去产品中该杂质的方法是:______.
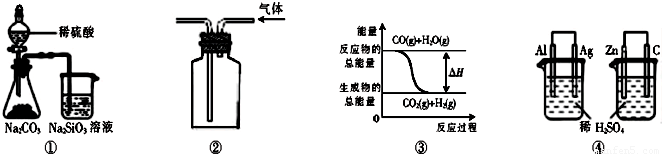
某研究性学习小组在网上收集到如下信息:钾、钙、钠、镁等活泼金属都能在CO2气体中燃烧.他们对钠在CO2气体中燃烧后的产物中的白色物质进行了如下探究:
【实验】将燃烧的钠迅速伸入到盛有装满CO2的集气瓶中,钠在其中继续燃烧,反应后冷却,瓶底附着黑色颗粒,瓶壁上粘附着白色物质.
(1)通过钠在CO2气体中燃烧的实验,你认为燃烧的条件是______.
(2)燃烧的本质是______.
(3)2010年8月初发生的俄罗斯森林大火有比伦敦市还要大的面积.控制森林火灾是世界性难题.根据燃烧的条件,请你解释为什么设置森林防火隔离带能有效阻止森林火灾的蔓延?______.
【提出假设】假设1:白色物质是Na2O.
假设2:白色物质是Na2CO3.
假设3:白色物质是Na2O和Na2CO3的混合物.
【设计实验方案.验证假设】该小组对燃烧后的白色产物进行如下探究:
【思考与交流】
(4)甲同学认为方案1得到的结论不正确,其理由是______.
(5)乙同学认为方案2得到的结论正确,白色物质为______.
(6)通过方案1和方案2的实验,你认为上述三个假设中,______成立.你的理由是______.
(7)钠在二氧化碳中燃烧的化学方程式为______ 2Na2CO3+C
0 67399 67407 67413 67417 67423 67425 67429 67435 67437 67443 67449 67453 67455 67459 67465 67467 67473 67477 67479 67483 67485 67489 67491 67493 67494 67495 67497 67498 67499 67501 67503 67507 67509 67513 67515 67519 67525 67527 67533 67537 67539 67543 67549 67555 67557 67563 67567 67569 67575 67579 67585 67593 203614
【实验】将燃烧的钠迅速伸入到盛有装满CO2的集气瓶中,钠在其中继续燃烧,反应后冷却,瓶底附着黑色颗粒,瓶壁上粘附着白色物质.
(1)通过钠在CO2气体中燃烧的实验,你认为燃烧的条件是______.
(2)燃烧的本质是______.
(3)2010年8月初发生的俄罗斯森林大火有比伦敦市还要大的面积.控制森林火灾是世界性难题.根据燃烧的条件,请你解释为什么设置森林防火隔离带能有效阻止森林火灾的蔓延?______.
【提出假设】假设1:白色物质是Na2O.
假设2:白色物质是Na2CO3.
假设3:白色物质是Na2O和Na2CO3的混合物.
【设计实验方案.验证假设】该小组对燃烧后的白色产物进行如下探究:
| 实验方案 | 实验操作 | 实验现象 | 结论 |
| 方案1 | 取少量白色物质于试管中,加入适量水,振荡,样品全部溶于水,向其中加入无色酚酞试液 | 溶液变成红色 | 白色物质为Na2O |
| 方案2 | ①取少量白色物质于试管中,加入适量水,振荡,样品全部溶于水,向其中加入过量的CaCl2溶液 | 出现白色沉淀 | |
| ③静置片刻,取上层清液于试管中,滴加无色酚酞试液 | 无明显现象 |
(4)甲同学认为方案1得到的结论不正确,其理由是______.
(5)乙同学认为方案2得到的结论正确,白色物质为______.
(6)通过方案1和方案2的实验,你认为上述三个假设中,______成立.你的理由是______.
(7)钠在二氧化碳中燃烧的化学方程式为______ 2Na2CO3+C
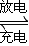 Li2S2O4.下列说法正确的是( )
Li2S2O4.下列说法正确的是( )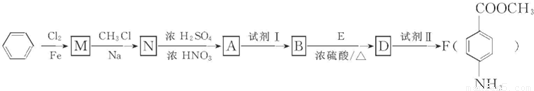
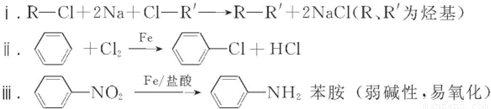
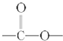 结构.______
结构.______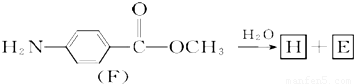 化合物H在一定条件下经缩聚反应可制得高分子纤维,广泛用于通讯、导弹、宇航等领域.请写出该缩聚反应的化学方程式:
化合物H在一定条件下经缩聚反应可制得高分子纤维,广泛用于通讯、导弹、宇航等领域.请写出该缩聚反应的化学方程式: