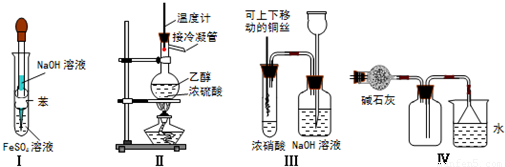
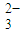工业合成氨与制备硝酸一般可连续生产,流程如下:
(1)某温度下体积为200L的氨合成塔中,测得如下数据:
根据表中数据计算0~2小时内N2的平均反应速率 mol?L-1?h-1
若起始时与平衡时的压强之比为a,则N2的转化率为 (用含a的代数式表示)
(2)希腊阿里斯多德大学的 George Marnellos 和 Michael Stoukides,发明了一种合成氨的新方法(Science,2,Oct.1998,p98),在常压下,把氢气和用氦气稀释的氮气分别通入一个加热到570℃的电解池,利用能通过氢离子的多孔陶瓷固体作电解质,氢气和氮气在电极上合成了氨,转化率达到78%,试写出电解池阴极的电极反应式
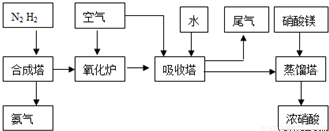
(3)氨气和氧气从145℃就开始反应,在不同温度和催化剂条件下生成不同产物(如图):
4NH3+5O2?4NO+6H2O K1=1×1053(900℃)
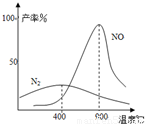
4NH3+3O2?2N2+6H2O K2=1×1067(900℃)温度较低时以生成 为主,温度高于900℃时,NO产率下降的原因 .吸收塔中需要补充空气的原因 .
(4)尾气处理时小型化工厂常用尿素作为氮氧化物的吸收剂,此法运行费用低,吸收效果好,不产生二次污染,吸收后尾气中NOx的去除率高达99.95%.其主要的反应为氮氧化物混合气与水反应生成亚硝酸,亚硝酸再与尿素反应生成CO2和N2请写出有关反应化学方程式 , .

(1)某温度下体积为200L的氨合成塔中,测得如下数据:
| 时间(h)浓度(mol/L) | 1 | 2 | 3 | 4 | |
| N2 | 1.500 | 1.400 | 1.200 | C1 | C1 |
| H2 | 4.500 | 4.200 | 3.600 | C2 | C2 |
| NH3 | 0.200 | 0.600 | C3 | C3 |
若起始时与平衡时的压强之比为a,则N2的转化率为 (用含a的代数式表示)
(2)希腊阿里斯多德大学的 George Marnellos 和 Michael Stoukides,发明了一种合成氨的新方法(Science,2,Oct.1998,p98),在常压下,把氢气和用氦气稀释的氮气分别通入一个加热到570℃的电解池,利用能通过氢离子的多孔陶瓷固体作电解质,氢气和氮气在电极上合成了氨,转化率达到78%,试写出电解池阴极的电极反应式
(3)氨气和氧气从145℃就开始反应,在不同温度和催化剂条件下生成不同产物(如图):
4NH3+5O2?4NO+6H2O K1=1×1053(900℃)
4NH3+3O2?2N2+6H2O K2=1×1067(900℃)温度较低时以生成 为主,温度高于900℃时,NO产率下降的原因 .吸收塔中需要补充空气的原因 .
(4)尾气处理时小型化工厂常用尿素作为氮氧化物的吸收剂,此法运行费用低,吸收效果好,不产生二次污染,吸收后尾气中NOx的去除率高达99.95%.其主要的反应为氮氧化物混合气与水反应生成亚硝酸,亚硝酸再与尿素反应生成CO2和N2请写出有关反应化学方程式 , .

用如图所示装置进行下列实验,放置一段时间后,实验结果与预测的现象不一致的是( )
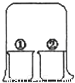
A.A
B.B
C.C
D.D
0 67351 67359 67365 67369 67375 67377 67381 67387 67389 67395 67401 67405 67407 67411 67417 67419 67425 67429 67431 67435 67437 67441 67443 67445 67446 67447 67449 67450 67451 67453 67455 67459 67461 67465 67467 67471 67477 67479 67485 67489 67491 67495 67501 67507 67509 67515 67519 67521 67527 67531 67537 67545 203614
| ①中的物质 | ②中的物质 | 预测现象 | |
| A | 浓盐酸 | 浓氨水 | 装置内出现白烟 |
| B | 酚酞溶液 | 浓硝酸 | ①中溶液变红 |
| C | 淀粉KI溶液 | 饱和氯水 | ①中溶液变蓝 |
| D | 饱和硫酸铜溶液 | 浓硫酸 | ①中溶液析出蓝色晶体 |

A.A
B.B
C.C
D.D
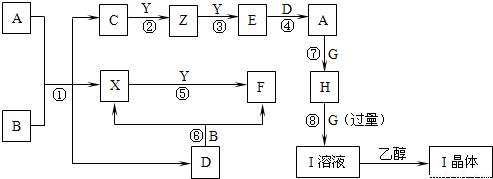
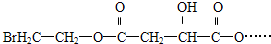
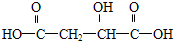 试回答:
试回答: .
. CaC2+CO
CaC2+CO Mg2C3+2CO
Mg2C3+2CO 2CO)
2CO)
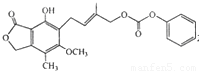 最多能与“mo1 NaOH的水溶液完全反应
最多能与“mo1 NaOH的水溶液完全反应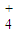 、SO
、SO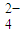 、Cl-
、Cl-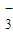 、Cl-
、Cl-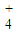 、Na+、OH-、SiO
、Na+、OH-、SiO