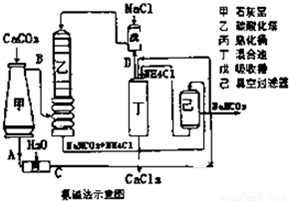
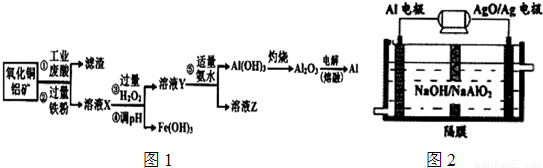
利用工业废酸(含10%H2SO4)处理废弃氧化铜铝矿(含CuO、Al2O3及不溶性杂质,且杂质不参与反应)冶炼铝的主要流程如图1:
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH,见下表:
回答下列问题:
(1)操作②中的离子方程式为______,操作⑤中生成沉淀的离子方程式为______.
(2)操作③中加入过量的H2O2的目的是______.
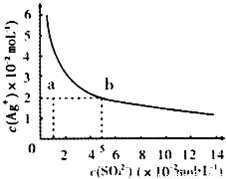
(3)若Z溶液pH=5(25°C),则溶液中c(NH4+)与c(SO42-)的大小关系为______..
(4)Al-AgO池是一种新型电源,其原理如图2所示:该电池负极反应式为:______.
(5)以熔融盐为电镀液可以在钢材表面镀铝,镀铝电解池中.金属铝为______极;镀铝后能防止钢材腐蚀,其原因是______.
0 66901 66909 66915 66919 66925 66927 66931 66937 66939 66945 66951 66955 66957 66961 66967 66969 66975 66979 66981 66985 66987 66991 66993 66995 66996 66997 66999 67000 67001 67003 67005 67009 67011 67015 67017 67021 67027 67029 67035 67039 67041 67045 67051 67057 67059 67065 67069 67071 67077 67081 67087 67095 203614
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH,见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | AlOH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
(1)操作②中的离子方程式为______,操作⑤中生成沉淀的离子方程式为______.
(2)操作③中加入过量的H2O2的目的是______.
(3)若Z溶液pH=5(25°C),则溶液中c(NH4+)与c(SO42-)的大小关系为______..
(4)Al-AgO池是一种新型电源,其原理如图2所示:该电池负极反应式为:______.
(5)以熔融盐为电镀液可以在钢材表面镀铝,镀铝电解池中.金属铝为______极;镀铝后能防止钢材腐蚀,其原因是______.

 O2(g)═CO2(g)△H2=-283KJ?mol-1
O2(g)═CO2(g)△H2=-283KJ?mol-1 O2(g)═H2O(g)△H3=-242KJ?mol-1
O2(g)═H2O(g)△H3=-242KJ?mol-1 O2(g)═H2O(g)△H4=-286KJ?mol-1
O2(g)═H2O(g)△H4=-286KJ?mol-1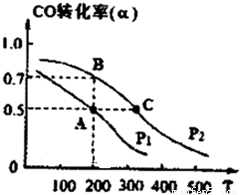
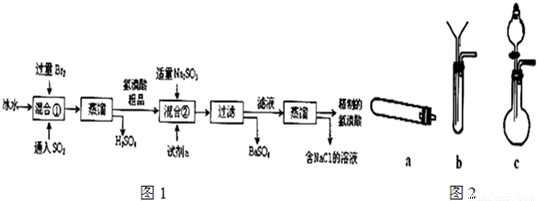
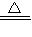 2NaHSO4+MnSO4+Br2↑+2H2O 制取Br2最好选用下列装置中的______ (填写字母,固定和加热装置均已省略).简述检验图2装置气密性的方法______.
2NaHSO4+MnSO4+Br2↑+2H2O 制取Br2最好选用下列装置中的______ (填写字母,固定和加热装置均已省略).简述检验图2装置气密性的方法______.