题目内容
请运用化学反应原理的相关知识研究元素及其化合物的性质.(1)工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:
CO(g)+2H2(g)?CH3OH(g)△H1=-116KJ?mol-1
又知:CO(g)+
 O2(g)═CO2(g)△H2=-283KJ?mol-1
O2(g)═CO2(g)△H2=-283KJ?mol-1H2(g)+
 O2(g)═H2O(g)△H3=-242KJ?mol-1
O2(g)═H2O(g)△H3=-242KJ?mol-1H2(g)+
 O2(g)═H2O(g)△H4=-286KJ?mol-1
O2(g)═H2O(g)△H4=-286KJ?mol-1则甲醇的燃烧热为______.
(2)T℃时,向2L密闭容器中充入4mol CO和6mol H2,5min后达平衡时CH3OH物质的量为2mol.该反应的速率v(H2)为______;下列措施中有利于增大该反应的反应速率且提高转化率的是______.
a.随时将CH3OH与反应混合物分离
b.降低反应温度
c.使用高效催化剂
d.增大体系压强
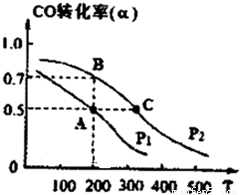
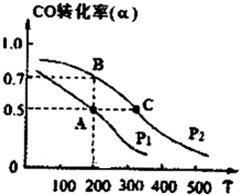
(3)在密闭容器中充有10mol CO与20mol H2,在催化剂作用下反应生成甲醇,CO的转化率(a)与温度(T)、压强(P)的关系如图所示.
①A、C两点都表示达到的平衡状态,则自反应开始到达平衡状态所需的时间,tA______tc(填“大于”、“小于’’或“等于“).
②若A点时容器的体积为10L,该温度下B点的平衡常数K=______.
(4)Na2SO3的水溶液呈______(填“酸”、“中”、‘‘碱”)性,原因是(用离子方程式表示):______;把CaCO3浊液滴入l.0mol/L的Na2SO3溶液中,能否产生CaSO3沉淀?若不能,说明原因;若可行,请简述判断依据及转化过程______
(已知:Ksp(CaSO3)=1.4×10-7,Ksp(CaCO3)=2.8×10-9).
(2)根据速率公式计算出v(CH3OH),然后根据反应速率之比等于化学计量数之比计算氢气的反应速率;
根据外界条件(压强、温度、浓度以及使用催化剂)对化学反应速率的影响解答;
提高反应物的转化率,应使平衡向正反应方向移动,结合方程式的特点和影响化学平衡的条件(压强、温度、浓度)来解答;
(3)①根据温度对反应的影响来判断,温度越高,反应速率越大;
②根据图象判断出平衡时的各种物质的浓度,用平衡常数的表达式进行计算;
(4)Na2SO3为强碱弱酸盐,亚硫酸根离子水解使溶液显碱性;根据Ksp(CaSO3)/Ksp(CaCO3)=50可知,当CaSO3与CaCO3的混合液中c(SO32-)>50c(CO32-)时,溶液中的c(Ca2+)与c(SO32-)之积大于Ksp(CaSO3),生成CaSO3沉淀,导致溶液中c(Ca2+)减小,使CaCO3的沉淀溶解平衡CaCO3?Ca2++CO32-,向着溶解的方向移动,导致CaCO3溶解,即发生由CaCO3向CaSO3的转变.
解答:解:(1)由①CO(g)+2H2(g)?CH3OH(g)△H1=-116kJ?mol-1
②CO(g)+
 O2(g)=CO2(g)△H2=-283kJ?mol-1
O2(g)=CO2(g)△H2=-283kJ?mol-1③H2(g)+
 O2(g)=H2O (l)△H3=-286kJ?mol-1
O2(g)=H2O (l)△H3=-286kJ?mol-1根据盖斯定律可知,②+③×2-①可得 CH3OH(g)+
 O2(g)=CO2(g)+2H2O (g)△H=(-283kJ?mol-1)+(-286kJ?mol-1)×2-(-116kJ?mol-1)=-739kJ?mol-1,
O2(g)=CO2(g)+2H2O (g)△H=(-283kJ?mol-1)+(-286kJ?mol-1)×2-(-116kJ?mol-1)=-739kJ?mol-1,故答案为:-739kJ?mol-1;
(2)由图象可知v(CH3OH)=
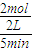 =0.2mol/(L?min),根据反应速率之比等于化学计量数之比可知v(H2)=2v(CH3OH)=2×0.25mol/(L?min)=0.4mol/(L?min),
=0.2mol/(L?min),根据反应速率之比等于化学计量数之比可知v(H2)=2v(CH3OH)=2×0.25mol/(L?min)=0.4mol/(L?min),a.随时将CH3OH与反应混合物分离,提高了反应物的转化率,但没有增大该反应的反应速率,故a错误;
b.降低反应温度,平衡正向移动,提高了反应物的转化率,但减小了该反应的反应速率,故b错误;
c.使用高效催化剂,平衡不移动,反应物的转化率不变,但提高该反应的反应速率,故c错误;
d.增大体系压强,平衡正向移动,提高了反应物的转化率,同时提高了该反应的反应速率,故d正确;
故答案为:0.4 mol(L?min)-1;d;
(3)①升高温度,反应速率增大,反应开始到达平衡状态所需的时间要少,所以反应开始到达平衡状态所需的时间tA 大于tC,故答案为:大于;
②根据图象可以看出,A点时CO的转化率为50%,则平衡时各物质的量浓度为:c(CO)=0.5mol/L;c(H2)=1mol/L;c(CH3OH)=0.5mol/L,所以平衡常数为K=
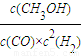 =
=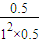 =1;故答案为:1;
=1;故答案为:1;(4)Na2SO3为强碱弱酸盐,亚硫酸根离子水解使溶液显碱性,水解离子反应为:SO32-+H2O?HSO3-+OH-,可行,判断依据是:由Ksp(CaSO3)/Ksp(CaCO3)=50知,当CaSO3与CaCO3的混合液中c(SO32-)>50c(CO32-)时,即发生由CaCO3向CaSO3的转变;转化过程为:把CaCO3浊液滴入0.1mol/L的Na2SO3溶液中时,溶液中的c(Ca2+)与c(SO32-)之积大于Ksp(CaSO3),生成CaSO3沉淀,导致溶液中c(Ca2+)减小,使CaCO3的沉淀溶解平衡CaCO3?Ca2++CO32-,向着溶解的方向移动,导致CaCO3溶解.
故答案为:碱;SO32-+H2O?HSO3-+OH-;可行,判断依据是:由Ksp(CaSO3)/Ksp(CaCO3)=50知,当CaSO3与CaCO3的混合液中c(SO32-)>50c(CO32-)时,即发生由CaCO3向CaSO3的转变;转化过程为:把CaCO3浊液滴入0.1mol/L的Na2SO3溶液中时,溶液中的c(Ca2+)与c(SO32-)之积大于Ksp(CaSO3),生成CaSO3沉淀,导致溶液中c(Ca2+)减小,使CaCO3的沉淀溶解平衡CaCO3?Ca2++CO32-,向着溶解的方向移动,导致CaCO3溶解.
点评:本题考查化学平衡的有关知识、盖斯定律以及盐类的水解,本题难度不大,做题时注意外界条件对化学反应速率和化学平衡的影响.

 全优点练单元计划系列答案
全优点练单元计划系列答案(1)近年来,我国储氢纳米碳管研究取得重大进展,用电弧法合成的碳纳米管中常伴有大量碳纳米颗粒(杂质),这种碳纳米颗粒可用氧化气化法提纯,其反应化学方程式为:
请完成并配平上述化学方程式.其中氧化剂是
(2)甲醇是一种新型燃料,甲醇燃料电池即将从实验室走向工业化生产.工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:CO(g)+2H2(g)?CH3OH(g)△H1=-116kJ?mol-1
①已知:CO(g)+
| 1 |
| 2 |
H2(g)+
| 1 |
| 2 |
则表示1mol气态甲醇完全燃烧生成CO2和水蒸气时的热化学方程式为
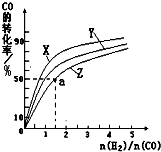
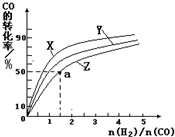
②在容积为1L的恒容容器中,分别研究在230℃、250℃、270℃三种温度下合成甲醇的规律.如图是上述三种温度下不同的H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系.
请回答:
ⅰ)在上述三种温度中,曲线Z对应的温度是
ⅱ)利用图中a点对应的数据,计算出曲线Z在对应温度下CO(g)+2H2(g)?CH3OH(g)的平衡常数K=
③在某温度下,将一定量的CO和H2投入10L的密闭容器中,5min时达到平衡,各物质的物质的浓度(mol?L-1)变化如下表所示:
| 0min | 5min | 10min | |
| CO | 0.1 | 0.05 | |
| H2 | 0.2 | 0.2 | |
| CH3OH | 0 | 0.04 | 0.05 |
(1)请完成该反应的化学方程式:(系数按顺序填在答题卷上)
(2)焦炭可用于制取水煤气.测得12g 碳与水蒸气完全反应生成水煤气时,吸收了131.6kJ热量.该反应的热化学方程式:
(3)活性炭可处理大气污染物NO.在2L密闭容器中加入NO和活性炭(无杂质),生成气体E和F,E和F均为空气的组成成分.当温度分别在T1和T2时,测得各物质平衡时物质的量如下表:
| 物质 温度 |
活性炭(mol) | NO(mol) | E(mol) | F(mol) |
| 初始 | 2.030 | 0.100 | 0 | 0 |
| T1 | 2.000 | 0.040 | 0.030 | 0.030 |
| T2 | 2.005 | 0.050 | 0.025 | 0.025 |
②根据上述信息判断,温度T1和T2的关系是(填序号)
a.T1>T2 b.T1<T2 c.无法比较
(4)CO2经常用氢氧化钠溶液来吸收,现有0.4molCO2,若用200mL 3mol/L NaOH溶液将其完全吸.回答下列问题:
①所得溶液的溶质是
②溶液中下列关系正确的是
a.c(Na+)>c(CO
2- 3 |
- 3 |
b.c(Na+)>c(HCO
- 3 |
2- 3 |
c.c(Na+)=2c(CO
2- 3 |
- 3 |
d.c(H+)+c(Na+)=c(OH-)+2c(CO
2- 3 |
- 3 |
(5)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp=3.8×10-9.CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的一定浓度的CaCl2溶液与Na2CO3溶液混合,若混合前Na2CO3溶液的浓度为1.9×10-4mol/L,则混合后若生成沉淀所需原CaCl2溶液的最小浓度为
(12分)欧盟原定于2012年1月1日起征收航空碳排税以应对冰川融化和全球变暖,使得对如何降低大气中CO2的含量及有效地开发利用碳资源的研究显得更加紧迫。请运用化学反应原理的相关知识研究碳及其化合物的性质
(1)用电弧法合成的储氢纳米碳管常伴有大量的碳纳米颗粒(杂质),这种颗粒可用如下氧化法提纯,请完成该反应的化学方程式:(系数按顺序填在答题卷上)
___ C+ ___ KMnO4+ ____ H2SO4→____CO2↑+ ____MnSO4 + ____K2SO4+ ____H2O
(2)活性炭可处理大气污染物NO。在2 L密闭容器中加入NO和活性炭(无杂质),生成气体E和F。当温度分别在T1和T2时,测得各物质平衡时物质的量如下表:
|
物质 n/mol T/℃ |
活性炭 |
NO |
E |
F |
|
初始 |
2.030 |
0.100 |
0 |
0 |
|
T1 |
2.000 |
0.040 |
0.030 |
0.030 |
|
T2 |
2.005 |
0.050 |
0.025 |
0.025 |
①请结合上表数据,写出NO与活性炭反应的化学方程式 。
②根据上述信息判断,温度T1和T2的关系是(填序号) 。
a.T1>T2 b.T1<T2 c.无法比较
(3)CO2经常用氢氧化钠来吸收,现有0.4molCO2,若用200ml 3mol/LNaOH溶液将其完全吸收,溶液中离子浓度由大到小的顺序为:
(4)CO还可以用做燃料电池的燃料,某熔融盐燃料电池具有高的发电效率,因而受到重视,该电池用 Li2CO3 和 Na2CO3 的熔融盐混合物作电解质, CO 为阳极燃气,空气与 CO2 的混和气为阴极助燃气,制得在 650 ℃下工作的燃料电池,其阳极反应式:2CO + 2CO32- =4CO2 +4e- 则 阴极反应式: ,电池总反应式: 。
 (2013?淄博一模)请运用化学反应原理的相关知识研究元素及其化合物的性质.
(2013?淄博一模)请运用化学反应原理的相关知识研究元素及其化合物的性质.