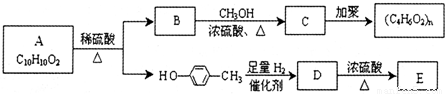
已知:短周期元素A、B、C、D、E原子序数依次增大.
(1)B、C、E三种元素组成的常见盐的水溶液呈酸性,原因是______(用离子方程式表示).
(2)常温下,若甲、丙两溶液的pH均等于5,则由水电离出的c(H+)甲:c(H+)丙=______;
(3)盐丙中含有的化学键是______.
(4)0.1mol D单质和0.2mol E单质组成的混合物投入到足量的A2C中,产生气体的体积(标准状况)是______.
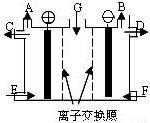
(5)反应:乙+C2→B2+A2C(未配平)可设计为燃料电池,则通入乙的电极是______极(填“正”或“负”),在碱性条件下其电极反应是______.
(6)已知xC和yC是C元素的两种核素,NA表示阿伏加德罗常数,下列说法正确的是______.
A.xC2与yC2互为同分异构体
B.xC与yC核外电子排布方式不同
C.通过化学变化可以实现xC与yC间的相互转化
D.标准状况下,1.12L xC2和1.12L yC2均含有0.1NA个C原子.
| 元素代号 | 相关信息 |
| A | A与C可形成A2C和A2C2两种化合物 |
| B | B的最高价氧化物对应的水化物甲与其气态氢化物乙反应可生成盐丙 |
| C | C的原子最外层电子数是其内层电子数的三倍 |
| D | D的单质能与冷水剧烈反应,得到强碱溶液 |
| E | 在第3周期元素中,E的简单离子半径最小 |
(2)常温下,若甲、丙两溶液的pH均等于5,则由水电离出的c(H+)甲:c(H+)丙=______;
(3)盐丙中含有的化学键是______.
(4)0.1mol D单质和0.2mol E单质组成的混合物投入到足量的A2C中,产生气体的体积(标准状况)是______.
(5)反应:乙+C2→B2+A2C(未配平)可设计为燃料电池,则通入乙的电极是______极(填“正”或“负”),在碱性条件下其电极反应是______.
(6)已知xC和yC是C元素的两种核素,NA表示阿伏加德罗常数,下列说法正确的是______.
A.xC2与yC2互为同分异构体
B.xC与yC核外电子排布方式不同
C.通过化学变化可以实现xC与yC间的相互转化
D.标准状况下,1.12L xC2和1.12L yC2均含有0.1NA个C原子.
A是由导热材料制成的钢化密闭容器,B是一耐化学腐蚀且易于传热的气球.关闭旋塞K.(已知:2NO2?N2O4;△H)
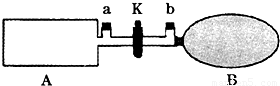
(1)若将一定量的NO2通过a充入A中,下表是该反应在不同温度下的化学平衡常数(K):
由表中数据判断△H 0(填“>”、“=”或“<”).
(2)若将等量的NO2通过a、b分别充入A、B中,反应起始时,A、B的体积相同.
一段时间后,反应达到平衡,此时A、B中生成的N2O4的速率是VA VB(填“>”、“<”、“=”);若打开旋塞K,气球B将 (填“变大”“变小”或“不变”).
(3)若在A、B中再充入与(2)中初始量相等的NO2,则达到平衡时,A中NO2的转化率将 (填“增大”“减小”或“不变”);若通入等量的Ne气,则达到平衡时,B中NO2的转化率将 (填“增大”“减小”或“不变”).
(4)室温下,若将等量的NO2通过a、b分别充入A、B中(关闭旋塞K),且A、B都保持体积不变,A套上一个绝热层,B与外界可以进行热传递,则达到平衡时, 中的颜色较深.

(1)若将一定量的NO2通过a充入A中,下表是该反应在不同温度下的化学平衡常数(K):
| 温度(K) | 273 | 308 | 373 |
| K-1 | 6.78 | 3.13 | 2.78 |
(2)若将等量的NO2通过a、b分别充入A、B中,反应起始时,A、B的体积相同.
一段时间后,反应达到平衡,此时A、B中生成的N2O4的速率是VA VB(填“>”、“<”、“=”);若打开旋塞K,气球B将 (填“变大”“变小”或“不变”).
(3)若在A、B中再充入与(2)中初始量相等的NO2,则达到平衡时,A中NO2的转化率将 (填“增大”“减小”或“不变”);若通入等量的Ne气,则达到平衡时,B中NO2的转化率将 (填“增大”“减小”或“不变”).
(4)室温下,若将等量的NO2通过a、b分别充入A、B中(关闭旋塞K),且A、B都保持体积不变,A套上一个绝热层,B与外界可以进行热传递,则达到平衡时, 中的颜色较深.
在实验室中用下列装置进行有关实验探究.请回答下列问题:
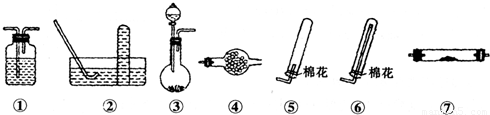
Ⅰ.气体制备时需检查装置的气密性,如下图所示各装置,肯定不符合气密性检查要求的是______.
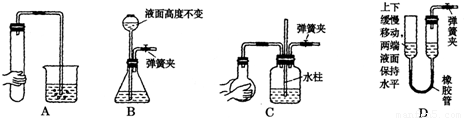
Ⅱ.若用下列装置③制取并收集干燥的NH3,烧瓶内装的试剂是______.收集装置应选择
______(填装置序号).证明氨气已收集满的操作是______.
Ⅲ.二氯化二硫(S2Cl2)在工业上用于橡胶的硫化.为在实验室合成S2Cl2,某化学研究性学习小组查阅了有关资料,得到如下信息:
①将干燥的氯气在110℃~140℃与硫反应,即可得S2Cl2粗品.
②有关物质的部分性质如下表:
设计实验装置图如下:
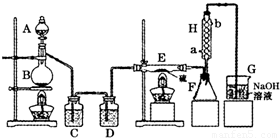
(1)B中反应的离子方程式:______ Mn2++Cl2↑+2H2O
0 66833 66841 66847 66851 66857 66859 66863 66869 66871 66877 66883 66887 66889 66893 66899 66901 66907 66911 66913 66917 66919 66923 66925 66927 66928 66929 66931 66932 66933 66935 66937 66941 66943 66947 66949 66953 66959 66961 66967 66971 66973 66977 66983 66989 66991 66997 67001 67003 67009 67013 67019 67027 203614
Ⅰ.气体制备时需检查装置的气密性,如下图所示各装置,肯定不符合气密性检查要求的是______.

Ⅱ.若用下列装置③制取并收集干燥的NH3,烧瓶内装的试剂是______.收集装置应选择
______(填装置序号).证明氨气已收集满的操作是______.

Ⅲ.二氯化二硫(S2Cl2)在工业上用于橡胶的硫化.为在实验室合成S2Cl2,某化学研究性学习小组查阅了有关资料,得到如下信息:
①将干燥的氯气在110℃~140℃与硫反应,即可得S2Cl2粗品.
②有关物质的部分性质如下表:
| 物质 | 熔点/℃ | 沸点℃ | 化学性质 |
| S | 112.8 | 444.6 | 略 |
| S2Cl2 | -77 | 137 | 遇水生成HCl,SO2,S;300℃以上完全分解; S2Cl2+Cl2 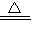 2SCl2 2SCl2 |

(1)B中反应的离子方程式:______ Mn2++Cl2↑+2H2O
 )+c(H2CO3)
)+c(H2CO3)