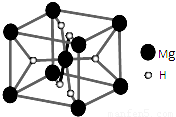
下列有关实验操作、现象和解释或结论都正确的是( )
A.A
B.B
C.C
D.D
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 将Cl2通入紫色石蕊试液中 | 石蕊试液先变红后褪色 | Cl2具有漂白性 |
| B | 向某溶液中先加入稀盐酸,后加入氯化钡溶液 | 先加稀盐酸无明显现象,后加氯化钡溶液,有白色沉淀生成 | 原溶液中存在SO42- |
| C | 铝箔插入浓硫酸中 | 无明显现象 | 铝与浓硫酸不反应 |
| D | 碘盐溶于水,在溶液中加入CCl4,振荡 | CCl4层显紫色 | 碘盐的成分是KI |
A.A
B.B
C.C
D.D
工业上“固定”和利用CO2能有效地减轻“温室效应”.
(1)目前工业上利用CO2来生产燃料甲醇,可将CO2变废为宝.已知常温常压下:
①CH3OH(l)+O2(g)═CO(g)+2H2O(g)△H=-354.8kJ/mol
②2CO(g)+O2(g)═2CO2(g)△H=-566kJ/mol
则反应2CO2(g)+4H2O(g)═2CH3OH(l)+3O2(g)△H=______kJ?mol-1
(2)T℃时,已知反应:CO2(g)+H2(g)?CO(g)+H2O(g)△H<0.在T℃下,将2mol CO2和2mol H2充入1L的密闭容器中,测得H2的物质的量随时间的变化情况如图中曲线I所示.
①按曲线I计算反应从0到4min时,υ(H2)=______.
②在T℃时,若仅改变某一外界条件时,测得H2的物质的量随时间的变化情况如图中曲线Ⅱ所示,则改变的外界条件为______.计算该反应按曲线II进行,达到平衡时,容器中c(CO2)=______.
(3)已知25℃时,乙酸和碳酸的电离平衡常数如下表:
①用饱和氨水吸收CO2可得到NH4HCO3溶液.若已知CH3COONH4溶液pH=7,则 NH4HCO3溶液显______(填“酸性”、“碱性”或“中性”).
②在25℃时,在乙酸溶液中加入一定量的NaHCO3,保持温度不变,所得混合液的pH=6,那么混合液中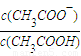 =______.
=______.
③向0.1mol?L -1CH3COOH溶液中加入少量CH3COONa晶体,保持温度不变,下列有关说法正确的是______(填代号).
a.溶液的pH增大 b.CH3COOH的电离程度增大
c.溶液的导电能力减弱 d.溶液中c(OH-)?c(H+)不变.

0 66800 66808 66814 66818 66824 66826 66830 66836 66838 66844 66850 66854 66856 66860 66866 66868 66874 66878 66880 66884 66886 66890 66892 66894 66895 66896 66898 66899 66900 66902 66904 66908 66910 66914 66916 66920 66926 66928 66934 66938 66940 66944 66950 66956 66958 66964 66968 66970 66976 66980 66986 66994 203614
(1)目前工业上利用CO2来生产燃料甲醇,可将CO2变废为宝.已知常温常压下:
①CH3OH(l)+O2(g)═CO(g)+2H2O(g)△H=-354.8kJ/mol
②2CO(g)+O2(g)═2CO2(g)△H=-566kJ/mol
则反应2CO2(g)+4H2O(g)═2CH3OH(l)+3O2(g)△H=______kJ?mol-1
(2)T℃时,已知反应:CO2(g)+H2(g)?CO(g)+H2O(g)△H<0.在T℃下,将2mol CO2和2mol H2充入1L的密闭容器中,测得H2的物质的量随时间的变化情况如图中曲线I所示.
①按曲线I计算反应从0到4min时,υ(H2)=______.
②在T℃时,若仅改变某一外界条件时,测得H2的物质的量随时间的变化情况如图中曲线Ⅱ所示,则改变的外界条件为______.计算该反应按曲线II进行,达到平衡时,容器中c(CO2)=______.
(3)已知25℃时,乙酸和碳酸的电离平衡常数如下表:
| 物质的化学式 | CH3COOH | H2CO3 | |
| 电离平衡常数 | K=1.8×10-5 | K1=4.3×10-7 | K2=5.6×10-11 |
②在25℃时,在乙酸溶液中加入一定量的NaHCO3,保持温度不变,所得混合液的pH=6,那么混合液中
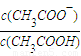 =______.
=______.③向0.1mol?L -1CH3COOH溶液中加入少量CH3COONa晶体,保持温度不变,下列有关说法正确的是______(填代号).
a.溶液的pH增大 b.CH3COOH的电离程度增大
c.溶液的导电能力减弱 d.溶液中c(OH-)?c(H+)不变.

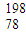 Pt和
Pt和 Pt是中子数不同、质子数相同的同种核素
Pt是中子数不同、质子数相同的同种核素

 Na2S4+3NaBr
Na2S4+3NaBr