下列物质、类别、用途或储存方法对应关系正确的是( )
A.A
B.B
C.C
D.D
| A、Na2CO3 | B、CH3COOH | C、NH3?H2O | D、Na2SiO3 |
| 碱 | 弱电解质 | 混合物 | 正盐 |
 烧碱工业 |  制食醋 |  棕色瓶密封保存 |  带玻璃塞的试剂瓶 |
A.A
B.B
C.C
D.D
下列有关实验操作、现象和解释或结论都正确的是( )
A.A
B.B
C.C
D.D
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 溶液中加入HCl无现象,再滴加BaCl2溶液 | 有白色沉淀生成 | 原溶液中有SO42- |
| B | AgI沉淀中滴入稀KCl溶液 | 有白色沉淀出现 | AgCl比AgI更难溶 |
| C | 向CH3CH2X中加入少量AgNO3溶液,加热 | 有浅黄色沉淀生成 | CH3CH2X中含有Br- |
| D | 向淀粉溶液中加入稀H2SO4,加热几分钟,冷却后再加入新制Cu(OH)2浊液,加热, | 没有红色沉淀生成 | 淀粉没有水解成葡萄糖 |
A.A
B.B
C.C
D.D
一定条件下,向密闭容器中加入 X物质,发生反应3X(g)?Y(g)+Z(g)△H<0,反应一定时间后改变某一个外界条件,反应中各时刻X物质的浓度如下表所示,下列说法中不正确的是( )
A.0~5min时,该反应的速率为v(X)=0.12 mol/
B.5min时反应达到第一次平衡,该温度下的平衡常数数值为0.625
C.15min时改变的条件不可能是升高温度
D.从初始到18min时,X的转化率为30%
| 反应时间(min) | 5 | 15 | 17 | 20 | |
| X的浓度(mol/L) | 1.0 | 0.4 | 0.4 | 0.7 | 0.7 |
A.0~5min时,该反应的速率为v(X)=0.12 mol/
B.5min时反应达到第一次平衡,该温度下的平衡常数数值为0.625
C.15min时改变的条件不可能是升高温度
D.从初始到18min时,X的转化率为30%
下表为元素周期表的一部分,请参照①-⑨相关元素在表中的位置,用化学用语回答下列问题:
(1)④、⑤、⑥的原子半径由大到小的顺序为______.
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是______.
(3)由②④⑤三种元素组成的物质的水溶液显碱性,用离子方程式表示溶液显碱性的原因:______
(4)甲、乙是由②③④三种元素中一种或两种元素形成的双原子分子或负二价阴离子,它们的电子总数相等,甲与钙元素组成的化合物既含离子键又含非极性共价键,则该化合物的电子式为:______,乙是一种常用的还原剂,请用化学方程式表示它在工业上的一种重要用途:______ 2Fe+3CO2
0 66789 66797 66803 66807 66813 66815 66819 66825 66827 66833 66839 66843 66845 66849 66855 66857 66863 66867 66869 66873 66875 66879 66881 66883 66884 66885 66887 66888 66889 66891 66893 66897 66899 66903 66905 66909 66915 66917 66923 66927 66929 66933 66939 66945 66947 66953 66957 66959 66965 66969 66975 66983 203614
| 族 周期 | ⅠA | |||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | |||||
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是______.
(3)由②④⑤三种元素组成的物质的水溶液显碱性,用离子方程式表示溶液显碱性的原因:______
(4)甲、乙是由②③④三种元素中一种或两种元素形成的双原子分子或负二价阴离子,它们的电子总数相等,甲与钙元素组成的化合物既含离子键又含非极性共价键,则该化合物的电子式为:______,乙是一种常用的还原剂,请用化学方程式表示它在工业上的一种重要用途:______ 2Fe+3CO2
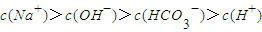
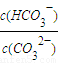 减小
减小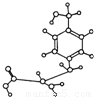
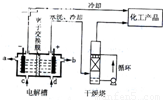
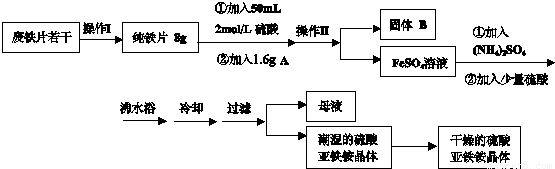
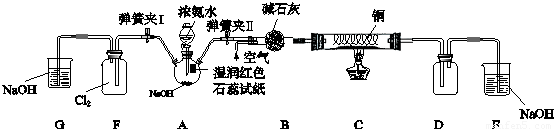
 3Cu+N2+3H2O
3Cu+N2+3H2O