一定温度下,在2L密闭容器中加入纳米级Cu2O并通入0.1mol H2O(g),发生反应:2H2O(g)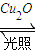 2H2(g)+O2(g),△H=+484kJ?mol-1,不同时间产生O2的物质的量见下表:
2H2(g)+O2(g),△H=+484kJ?mol-1,不同时间产生O2的物质的量见下表:
下列说法正确的是( )
A.前20min的反应速率v(H2O)=2.5×10-5mol?L-1?min-1
B.达平衡时,至少需要从外界吸收的能量为0.968kJ
C.增大c(H2O),可以提高水的分解率
D.催化效果与Cu2O颗粒的大小有关
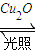 2H2(g)+O2(g),△H=+484kJ?mol-1,不同时间产生O2的物质的量见下表:
2H2(g)+O2(g),△H=+484kJ?mol-1,不同时间产生O2的物质的量见下表:| 时间/min | 20 | 40 | 60 | 80 |
| n(O2)/moL | 0.0010 | 0.0016 | 0.0020 | 0.0020 |
A.前20min的反应速率v(H2O)=2.5×10-5mol?L-1?min-1
B.达平衡时,至少需要从外界吸收的能量为0.968kJ
C.增大c(H2O),可以提高水的分解率
D.催化效果与Cu2O颗粒的大小有关
硝酸铝广泛用于有机合成、印染工业等.工业上以铝灰为原料(主要成分为Al,含少量Al2O3、Fe2O3、SiO2、CaO、MgO等)制备硝酸铝的工艺流程如下:

已知:Al(OH)3沉淀和溶解的pH如下表:
回答下列问题:
(1)碱溶时,发生主反应的离子方程式为______.
(2)工艺流程中第一次加入硝酸调pH=7.0的目的是______.pH=7.0时,溶液中c(Al3+)=______(通常条件下,Ksp[Al(OH)3]=1.3×10-33).
(3)若忽略杂质跟酸、碱的反应,则在碱溶、调pH=7.0、酸溶过程中,理论上消耗碱、酸的物质的量之比n1(NaOH):n2(HNO3):n3(HNO3)=______.
(4)现用1t铝灰制硝酸铝晶体[Al(NO3)3?9H2O],最后生产出7.5t硝酸铝晶体.若生产过程中铝元素的损失率为10%,计算铝灰中铝元素的质量分数.
0 66744 66752 66758 66762 66768 66770 66774 66780 66782 66788 66794 66798 66800 66804 66810 66812 66818 66822 66824 66828 66830 66834 66836 66838 66839 66840 66842 66843 66844 66846 66848 66852 66854 66858 66860 66864 66870 66872 66878 66882 66884 66888 66894 66900 66902 66908 66912 66914 66920 66924 66930 66938 203614

已知:Al(OH)3沉淀和溶解的pH如下表:
| Al(OH)3 | 开始沉淀 | 沉淀完全 | 沉淀开始溶解 | 沉淀完全溶解 |
| pH | 3.3 | 5.0 | 7.8 | 12.8 |
(1)碱溶时,发生主反应的离子方程式为______.
(2)工艺流程中第一次加入硝酸调pH=7.0的目的是______.pH=7.0时,溶液中c(Al3+)=______(通常条件下,Ksp[Al(OH)3]=1.3×10-33).
(3)若忽略杂质跟酸、碱的反应,则在碱溶、调pH=7.0、酸溶过程中,理论上消耗碱、酸的物质的量之比n1(NaOH):n2(HNO3):n3(HNO3)=______.
(4)现用1t铝灰制硝酸铝晶体[Al(NO3)3?9H2O],最后生产出7.5t硝酸铝晶体.若生产过程中铝元素的损失率为10%,计算铝灰中铝元素的质量分数.
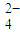 等)为原料制备亚氯酸钠(NaClO2)的工艺如下(试剂A为依次加入的过量BaCl2、NaOH、Na2CO3溶液):
等)为原料制备亚氯酸钠(NaClO2)的工艺如下(试剂A为依次加入的过量BaCl2、NaOH、Na2CO3溶液):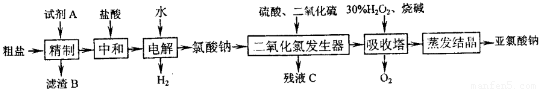
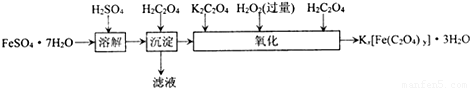
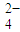 含量的实验步骤如下:
含量的实验步骤如下: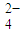 全部氧化成CO2,Fe2+全部氧化成Fe3+记录体积.
全部氧化成CO2,Fe2+全部氧化成Fe3+记录体积.