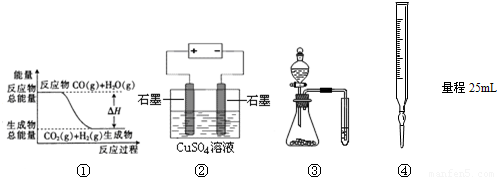
大气中的部分碘源于O3对海水中I-的氧化.将O3持续通入NaI溶液中进行模拟研究.
(1)O3将I-氧化成I2的过程由3步反应组成:
①I-(aq)+O3(g)=IO-(aq)+O2(g)△H1
②IO-(aq)+H+(aq)?HOI(aq)△H2
③HOI(aq)+I-(aq)+H+(aq)?I2(aq)+H2O(l)△H3
总反应的化学方程式为 ,其反应△H=
(2)在溶液中存在化学平衡:I2(aq)+I-(aq)?I3-(aq),其平衡常数表达式为 .
(3)为探究Fe2+对O3氧化I-反应的影响(反应体系如图1),某研究小组测定两组实验中I3-浓度和体系pH,结果见图2和下表.
第1组实验中,导致反应后pH升高的原因是 .
②图1中的A为 ,由Fe3+生成A的过程能显著提高Ⅰ-的转化率,原因是 .
③第2组实验进行18s后,I3-浓度下降.导致下降的直接原因有(双选) .
A.c(H+)减小 B.c(I-)减小 C.I2(g)不断生成 D.c(Fe3+)增加
(4)据图2,计算3-18s内第2组实验中生成I3-的平均反应速率(写出计算过程,结果保留两位有效数字).
0 66676 66684 66690 66694 66700 66702 66706 66712 66714 66720 66726 66730 66732 66736 66742 66744 66750 66754 66756 66760 66762 66766 66768 66770 66771 66772 66774 66775 66776 66778 66780 66784 66786 66790 66792 66796 66802 66804 66810 66814 66816 66820 66826 66832 66834 66840 66844 66846 66852 66856 66862 66870 203614
(1)O3将I-氧化成I2的过程由3步反应组成:
①I-(aq)+O3(g)=IO-(aq)+O2(g)△H1
②IO-(aq)+H+(aq)?HOI(aq)△H2
③HOI(aq)+I-(aq)+H+(aq)?I2(aq)+H2O(l)△H3
总反应的化学方程式为 ,其反应△H=
(2)在溶液中存在化学平衡:I2(aq)+I-(aq)?I3-(aq),其平衡常数表达式为 .
(3)为探究Fe2+对O3氧化I-反应的影响(反应体系如图1),某研究小组测定两组实验中I3-浓度和体系pH,结果见图2和下表.

| 编号 | 反应物 | 反应前pH | 反应后pH |
| 第1组 | O3+I- | 5.2 | 11.0 |
| 第2组 | O3+I-+Fe2- | 5.2 | 4.1 |
②图1中的A为 ,由Fe3+生成A的过程能显著提高Ⅰ-的转化率,原因是 .
③第2组实验进行18s后,I3-浓度下降.导致下降的直接原因有(双选) .
A.c(H+)减小 B.c(I-)减小 C.I2(g)不断生成 D.c(Fe3+)增加
(4)据图2,计算3-18s内第2组实验中生成I3-的平均反应速率(写出计算过程,结果保留两位有效数字).
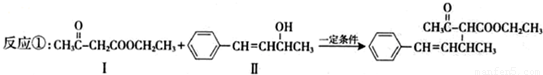
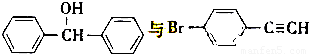 ,也可以发生类似反应①的反应,有机产物的结构简式为 .
,也可以发生类似反应①的反应,有机产物的结构简式为 .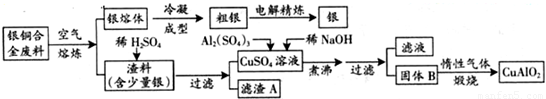
 CuAlO2+ ↑
CuAlO2+ ↑
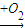 氧化物
氧化物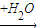 酸或碱
酸或碱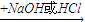 盐.
盐.