氧化铜有多种用途,如用作玻璃着色剂,油类脱硫剂等,为获得纯净的氧化铜并探究其性质,某同学查找了溶度积数据并通过计算得到有关信息(如表),用工业硫酸铜(含硫酸亚铁等杂质)进行如下实验:
㈠制备氧化铜
工业CuSO4
 CuSO4溶液
CuSO4溶液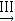 CuSO4?5H2O…CuO
CuSO4?5H2O…CuO
(1)步骤Ⅰ的操作是加入水和少量硫酸溶解样品并过滤,目的是除去不溶性杂质,这一步骤中加酸的作用是______.
(2)步骤Ⅱ的操作是:滴加H2O2溶液,稍加热;待反应完全后,慢慢加入Cu2(OH)2CO3粉末,搅拌,以控制溶液pH=3.5;加热煮沸一段时间,过滤,用稀硫酸酸化滤液至pH=1.
①这一步骤的目的是______,
②写出加入H2O2溶液时发生反应的离子方程式______
③控制溶液pH=3.5的目的是______,
(3)步骤Ⅲ的目的是得到CuSO4?5H2O晶体,操作是______,水浴加热烘干所得固体.水浴加热的特点是______.
㈡探究氧化铜性质
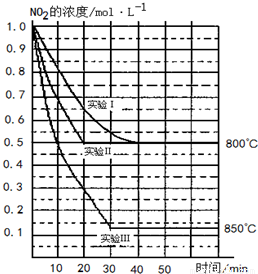
(1)取A、B两支试管,往A中先加入适量CuO粉末,再分别向A和B中加入等体积的3%H2O2溶液,只观察到A中有大量气泡,结论是______.
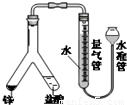
(2)为探究试管A中反应的速率,收集气体并测定其体积必需的实验仪器或装置为______.(填写序号)
0 66675 66683 66689 66693 66699 66701 66705 66711 66713 66719 66725 66729 66731 66735 66741 66743 66749 66753 66755 66759 66761 66765 66767 66769 66770 66771 66773 66774 66775 66777 66779 66783 66785 66789 66791 66795 66801 66803 66809 66813 66815 66819 66825 66831 66833 66839 66843 66845 66851 66855 66861 66869 203614
| 物 质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
| 完全沉淀时的pH范围 | ≥9.6 | ≥6.4 | 3~4 |
工业CuSO4
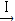
 CuSO4溶液
CuSO4溶液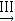 CuSO4?5H2O…CuO
CuSO4?5H2O…CuO(1)步骤Ⅰ的操作是加入水和少量硫酸溶解样品并过滤,目的是除去不溶性杂质,这一步骤中加酸的作用是______.
(2)步骤Ⅱ的操作是:滴加H2O2溶液,稍加热;待反应完全后,慢慢加入Cu2(OH)2CO3粉末,搅拌,以控制溶液pH=3.5;加热煮沸一段时间,过滤,用稀硫酸酸化滤液至pH=1.
①这一步骤的目的是______,
②写出加入H2O2溶液时发生反应的离子方程式______
③控制溶液pH=3.5的目的是______,
(3)步骤Ⅲ的目的是得到CuSO4?5H2O晶体,操作是______,水浴加热烘干所得固体.水浴加热的特点是______.
㈡探究氧化铜性质
(1)取A、B两支试管,往A中先加入适量CuO粉末,再分别向A和B中加入等体积的3%H2O2溶液,只观察到A中有大量气泡,结论是______.
(2)为探究试管A中反应的速率,收集气体并测定其体积必需的实验仪器或装置为______.(填写序号)

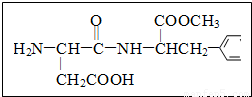

 (注:R、R´为烃基)
(注:R、R´为烃基)