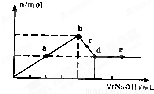
某同学用0.1082mol/L 的NaOH溶液滴定未知浓度的盐酸,以下是实验数据记录表.解答40-42小题:
(1)请根据如图(滴定管的局部)读出第2次实验的末读数,填充上表中的两个空格.
(2)列出求算待测盐酸溶液浓度的计算式(须含上表相关数据,不必计算结果)
(3)该同学欲测量一个玻璃容器的容积.他先量取20.00mL 3.820mol/L的H2SO4溶液注入该容器,加蒸馏水直至完全充满容器.待混合均匀后,从中取出25.00mL溶液置于锥形瓶中用0.1082mol/L 的NaOH溶液滴定,耗去碱液22.60mL.计算该玻璃容器的容积.

0 65343 65351 65357 65361 65367 65369 65373 65379 65381 65387 65393 65397 65399 65403 65409 65411 65417 65421 65423 65427 65429 65433 65435 65437 65438 65439 65441 65442 65443 65445 65447 65451 65453 65457 65459 65463 65469 65471 65477 65481 65483 65487 65493 65499 65501 65507 65511 65513 65519 65523 65529 65537 203614
| 实验序号 | 待测盐酸溶液的体积mL | 滴定管读数 | 消耗标准NaOH溶液的体积mL | |
| 初读数 | 末读数 | |||
| 1 | 20.00 | 0.00 | 19.90 | 19.90 |
| 2 | 20.00 | 0.05 | ||
(2)列出求算待测盐酸溶液浓度的计算式(须含上表相关数据,不必计算结果)
(3)该同学欲测量一个玻璃容器的容积.他先量取20.00mL 3.820mol/L的H2SO4溶液注入该容器,加蒸馏水直至完全充满容器.待混合均匀后,从中取出25.00mL溶液置于锥形瓶中用0.1082mol/L 的NaOH溶液滴定,耗去碱液22.60mL.计算该玻璃容器的容积.