下表是部分短周期元素的原子半径及主要化合价:
试回答下列问题:(1)七种元素中原子半径最大的元素在周期表中位置是 ;M在Z的最高价氧化物中燃烧的化学方程式为 .
(2)X可与R按1:1的原子个数比形成化合物甲,甲中存在的化学键有 ;X可与W组成含18电子的化合物乙,则乙的电子式为 .
| 元素代号 | W | R | X | Y | Z | Q | M |
| 原子半径/nm | 0.037 | 0.186 | 0.074 | 0.075 | 0.077 | 0.110 | 0.160 |
| 主要化合价 | +1 | +1 | -2 | -3,+5 | +2、+4 | -3、+5 | +2 |
(2)X可与R按1:1的原子个数比形成化合物甲,甲中存在的化学键有 ;X可与W组成含18电子的化合物乙,则乙的电子式为 .
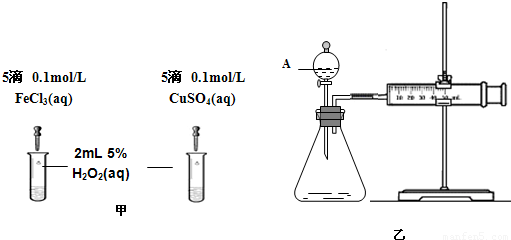
工业生产中常利用电解反应来制取新的物质.
(1)填写下表中用惰性电极电解各物质时阳极(和电源正极相连的极)、阴极(和电源负极相连的极)所得产物的化学式.
(2)请写出电解饱和食盐水时阳极上的电极反应式 .
(1)填写下表中用惰性电极电解各物质时阳极(和电源正极相连的极)、阴极(和电源负极相连的极)所得产物的化学式.
| 阳极产物 | 阴极产物 | |
| 饱和食盐水 | ||
| 氯化铜溶液 |
800℃时,在2L密闭容器内加入NO和O2,发生反应2NO(g)+O2(g) 2NO2(g),测得n(NO)随时间的变化如下表,请回答:
2NO2(g),测得n(NO)随时间的变化如下表,请回答:
(1)NO的平衡浓度c(NO)= ;
(2)用O2表示从0~2s内该反应的平均反应速率为 ;
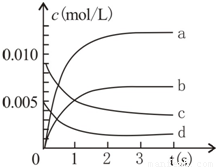
(3)右图中表示NO2变化的曲线是 ;
(4)能说明该反应已达到平衡状态的是 .
a.容器内NO、O2、NO2 物质的量之比为2:1:2
b.正反应和逆反应的速率都为0 c.容器内气体总物质的量保持不变
d.容器内气体的密度保持不变.
 2NO2(g),测得n(NO)随时间的变化如下表,请回答:
2NO2(g),测得n(NO)随时间的变化如下表,请回答:| 时间/s | 1 | 2 | 3 | 4 | 5 | |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(2)用O2表示从0~2s内该反应的平均反应速率为 ;
(3)右图中表示NO2变化的曲线是 ;
(4)能说明该反应已达到平衡状态的是 .
a.容器内NO、O2、NO2 物质的量之比为2:1:2
b.正反应和逆反应的速率都为0 c.容器内气体总物质的量保持不变
d.容器内气体的密度保持不变.

某学习小组研究同周期元素性质递变规律时,设计并进行了下列实验(表中的“实验步骤”与“实验现象”前后不一定是对应关系).
(1)请将各实验步骤对应的实验现象填写入下表中:
(2)此实验可得出的结论是:
金属性比较:______,非金属性比较:______;
(3)请写出反应②的离子方程式______.
0 65027 65035 65041 65045 65051 65053 65057 65063 65065 65071 65077 65081 65083 65087 65093 65095 65101 65105 65107 65111 65113 65117 65119 65121 65122 65123 65125 65126 65127 65129 65131 65135 65137 65141 65143 65147 65153 65155 65161 65165 65167 65171 65177 65183 65185 65191 65195 65197 65203 65207 65213 65221 203614
| 实验步骤 | 实验现象 |
| ①将镁条用砂纸打磨后,放入试管中,加入少量水后,加热至水沸腾;再向溶液中滴加酚酞溶液 | A.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变成红色. |
| ②向新制得的Na2S溶液中滴加新制的氯水 | B.有气体产生,溶液变成浅红色 |
| ③将一小块金属钠放入滴有酚酞溶液的冷水中 | C.剧烈反应,迅速产生大量无色气体 |
| ④将镁条投入稀盐酸中 | D.反应不十分剧烈;产生无色气体. |
| ⑤将铝条投入稀盐酸中 | E.生成白色胶状沉淀,继而沉淀消失 |
| ⑥向A1Cl3溶液中滴加NaOH溶液至过量 | F.生成淡黄色沉淀. |
| 实验步骤 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 实验现象(填A~F) | ▲ | ▲ | ▲ | C | D | ▲ |
金属性比较:______,非金属性比较:______;
(3)请写出反应②的离子方程式______.

 2H2↑+O2↑.制得的氢气可用于燃料电池.试回答下列问题:
2H2↑+O2↑.制得的氢气可用于燃料电池.试回答下列问题: