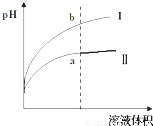
某校学生用中和滴定法测定某NaOH溶液的物质的量浓度,选甲基橙作指示剂.
(1)盛装0.2000mol/L盐酸标准液应该用______式滴定管.
(2)滴定时,左手控制滴定管,右手摇动锥形瓶,眼睛注视______.直到因加入一滴盐酸后,溶液由黄色变为橙色,并______为止.
(3)滴定操作可分解为如下几步:
①检查滴定管是否漏水;
②取一定体积的待测液于锥形瓶中;
③用标准溶液润洗盛标准溶液的滴定管,用待测液润洗盛待测液的滴定管
④装标准溶液和待测液并调整液面(记录初读数)
⑤用蒸馏水洗涤玻璃仪器
⑥滴定操作
正确的操作顺序为:______.
(4)有关数据记录如下:
则NaOH溶液的物质的量浓度为______mol/L.
(5)若只用蒸馏水冲洗锥形瓶,则测定结果______;若滴定前平视读数,滴定终点时俯视读数,则会使所测酸的浓度值______.(填“无影响”、“偏高”或“偏低”).
(1)盛装0.2000mol/L盐酸标准液应该用______式滴定管.
(2)滴定时,左手控制滴定管,右手摇动锥形瓶,眼睛注视______.直到因加入一滴盐酸后,溶液由黄色变为橙色,并______为止.
(3)滴定操作可分解为如下几步:
①检查滴定管是否漏水;
②取一定体积的待测液于锥形瓶中;
③用标准溶液润洗盛标准溶液的滴定管,用待测液润洗盛待测液的滴定管
④装标准溶液和待测液并调整液面(记录初读数)
⑤用蒸馏水洗涤玻璃仪器
⑥滴定操作
正确的操作顺序为:______.
(4)有关数据记录如下:
| 实验序号 | 待测液体积(mL) | 所消耗盐酸标准液的体积(mL) | |
| 滴定前 | 滴定后 | ||
| 1 | 20.00 | 0.50 | 20.70 |
| 2 | 20.00 | 6.00 | 26.00 |
| 3 | 20.00 | 1.40 | 21.20 |
(5)若只用蒸馏水冲洗锥形瓶,则测定结果______;若滴定前平视读数,滴定终点时俯视读数,则会使所测酸的浓度值______.(填“无影响”、“偏高”或“偏低”).
硫酸工业中SO2转化为SO3是重要的反应之一,在一定压强和催化剂作用下在2L密闭容器中充入0.8molSO2和2molO2发生反应:2SO2(g)+O2(g)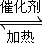 2SO3(g),SO2的转化率随温度的变化如下表所示:
2SO3(g),SO2的转化率随温度的变化如下表所示:
(1)由表中数据判断△H______0(填“>”、“=”或“<”)
(2)能判断该反应是否达到平衡状态的是______
A.容器的压强不变 B.混合气体的密度不变
C.混合气体中SO3的浓度不变 D.C(SO2)=C(SO3)
E.v正(SO2)=v正(SO3) F.v正(SO3)=2v逆(O2)
(3)某温度下经2min反应达到平衡后C(SO2)=0.08mol?L-1.
①0~2min之间,O2的反应速率为______.
②此时的温度为______℃.
③此温度下的平衡常数为______(可用分数表示).
(4)若将平衡反应混合物的压强增大(假如体积可变),平衡将______向移动.
0 63148 63156 63162 63166 63172 63174 63178 63184 63186 63192 63198 63202 63204 63208 63214 63216 63222 63226 63228 63232 63234 63238 63240 63242 63243 63244 63246 63247 63248 63250 63252 63256 63258 63262 63264 63268 63274 63276 63282 63286 63288 63292 63298 63304 63306 63312 63316 63318 63324 63328 63334 63342 203614
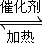 2SO3(g),SO2的转化率随温度的变化如下表所示:
2SO3(g),SO2的转化率随温度的变化如下表所示:| 温度°C | 450 | 500 | 550 | 600 |
| SO2的转化率% | 97.5 | 95.8 | 90.50 | 80.0 |
(2)能判断该反应是否达到平衡状态的是______
A.容器的压强不变 B.混合气体的密度不变
C.混合气体中SO3的浓度不变 D.C(SO2)=C(SO3)
E.v正(SO2)=v正(SO3) F.v正(SO3)=2v逆(O2)
(3)某温度下经2min反应达到平衡后C(SO2)=0.08mol?L-1.
①0~2min之间,O2的反应速率为______.
②此时的温度为______℃.
③此温度下的平衡常数为______(可用分数表示).
(4)若将平衡反应混合物的压强增大(假如体积可变),平衡将______向移动.