图a是1mol NO2和1mol CO反应生成CO2和NO过程中能量变化示意图,图b是反应中的CO和NO的浓度随时间变化的示意图.根据图意回答下列问题:
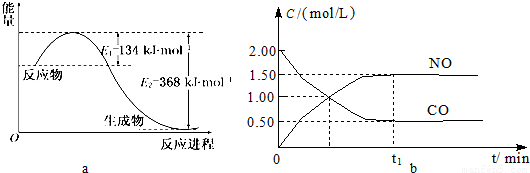
(1)写出NO2和CO反应的热化学方程式 .
(2)从反应开始到平衡,用NO2浓度变化表示平均反应速率v(NO2)= .
(3)此温度下该反应的平衡常数K= ;温度降低,K (填“变大”、“变小”或“不变”)
(4)若在温度和容积相同的三个密闭容器中,按不同方式投入反应物,测得反应达到平衡吋的有关数据如下表:
则:α1+α2= ,a+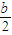 = ,m= .
= ,m= .

(1)写出NO2和CO反应的热化学方程式 .
(2)从反应开始到平衡,用NO2浓度变化表示平均反应速率v(NO2)= .
(3)此温度下该反应的平衡常数K= ;温度降低,K (填“变大”、“变小”或“不变”)
(4)若在温度和容积相同的三个密闭容器中,按不同方式投入反应物,测得反应达到平衡吋的有关数据如下表:
| 容 器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1mol NO2 1mol CO | 2mol NO 2mol CO2 | 1mol NO2、1mol CO 1mol NO、1mol CO2 |
| 平衡时c(NO)/mol?L-1 | 1.5 | 3 | m |
| 能量变化 | 放出a kJ | 吸收b kJ | 放出c kJ |
| CO或NO的转化率 | α1 | α2 | α3 |
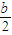 = ,m= .
= ,m= .
常温下,将某一元碱BOH和HCl溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
请回答:
(1)从第①组情况分析,BOH是 (选填“强碱”或“弱碱”).该组所得混合溶液中由水电离出的c(OH-)= mol?L-1.
(2)第②组情况表明,c 0.2.该混合液中离子浓度c(B+) c(Cl-)(选填“<”、“>”或“=”).
(3)从第③组实验结果分析,混合溶液中 (选填“<”、“>”或“=”)
甲:BOH的电离程度 BCl的水解程度;乙:c(B+)-2c (OH-) c(BOH)-2c(H+)
| 实验编号 | HCl的物质的量浓度 | BOH的物质的量浓度 | 混合溶液的pH |
| ① | 0.1 | 0.1 | pH=5 |
| ② | c | 0.2 | pH=7 |
| ③ | 0.1 | 0.2 | pH>7 |
(1)从第①组情况分析,BOH是 (选填“强碱”或“弱碱”).该组所得混合溶液中由水电离出的c(OH-)= mol?L-1.
(2)第②组情况表明,c 0.2.该混合液中离子浓度c(B+) c(Cl-)(选填“<”、“>”或“=”).
(3)从第③组实验结果分析,混合溶液中 (选填“<”、“>”或“=”)
甲:BOH的电离程度 BCl的水解程度;乙:c(B+)-2c (OH-) c(BOH)-2c(H+)
我国有丰富的天然气资源.以天然气为原料合成尿素的主要步骤如图所示(图中某些转化步骤及生成物未列出):

(1)“造合成气”发生的热化学方程式是CH4(g)+H2O(g)?CO(g)+3H2(g);△H>0
在恒温恒容的条件下,欲提高CH4的反应速率和转化率,下列措施可行的是 .
A、增大压强 B、升高温度 C、充入He气 D、增大水蒸气浓度
(2)“转化一氧化碳”发生的方程式是H2O(g)+CO(g)?H2(g)+CO2(g),该反应平衡常数随温度的变化如下:
提高氢碳比[n(H2O)/n(CO)],K值 (填“增大”、“不变”或“减小”);若该反应在400℃时进行,起始通入等物质的量的H2O和CO,反应进行到某一时刻时CO和CO2的浓度比为1:3,此时v(正) v(逆)(填“>”、“=”或“<”).
(3)有关合成氨工业的说法中正确的是 .
A、该反应属于人工固氮
B、合成氨工业中使用催化剂能提高反应物的利用率
C、合成氨反应温度控制在500℃左右,目的是使化学平衡向正反应方向移动
D、合成氨工业采用循环操作的主要原因是为了加快反应速率
(4)生产尿素过程中,理论上n(NH3):n(CO2)的最佳配比为 ,而实际生产过程中,往往使n(NH3):n(CO2)≥3,这是因为 .
(5)当甲烷合成氨气的转化率为60%时,以3.0×108L甲烷为原料能够合成 L 氨气.(假设体积均在标准状况下测定)
0 63098 63106 63112 63116 63122 63124 63128 63134 63136 63142 63148 63152 63154 63158 63164 63166 63172 63176 63178 63182 63184 63188 63190 63192 63193 63194 63196 63197 63198 63200 63202 63206 63208 63212 63214 63218 63224 63226 63232 63236 63238 63242 63248 63254 63256 63262 63266 63268 63274 63278 63284 63292 203614

(1)“造合成气”发生的热化学方程式是CH4(g)+H2O(g)?CO(g)+3H2(g);△H>0
在恒温恒容的条件下,欲提高CH4的反应速率和转化率,下列措施可行的是 .
A、增大压强 B、升高温度 C、充入He气 D、增大水蒸气浓度
(2)“转化一氧化碳”发生的方程式是H2O(g)+CO(g)?H2(g)+CO2(g),该反应平衡常数随温度的变化如下:
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
(3)有关合成氨工业的说法中正确的是 .
A、该反应属于人工固氮
B、合成氨工业中使用催化剂能提高反应物的利用率
C、合成氨反应温度控制在500℃左右,目的是使化学平衡向正反应方向移动
D、合成氨工业采用循环操作的主要原因是为了加快反应速率
(4)生产尿素过程中,理论上n(NH3):n(CO2)的最佳配比为 ,而实际生产过程中,往往使n(NH3):n(CO2)≥3,这是因为 .
(5)当甲烷合成氨气的转化率为60%时,以3.0×108L甲烷为原料能够合成 L 氨气.(假设体积均在标准状况下测定)

