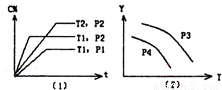
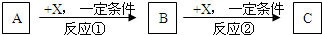
在恒容条件下化学反应:2SO2(g)+O2(g)?2SO3(g);△H=-QkJ?mol-1在上述条件下分别充入的气体和反应放出的热量(Q)如下表所列:根据以上数据,下列叙述正确的是( )
A.在上述条件下反应生成1mol SO3固体放热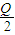 kJ
kJ
B.2Q3<2Q2=Q1<Q
C.Q1=2Q2=2Q3=Q
D.2Q2=2Q3<Q1<Q
| 容器 | SO2(mol) | O2(mol) | N2(mol) | Q(kJ) |
| 甲 | 2 | 1 | Q1 | |
| 乙 | 1 | 0.5 | Q2 | |
| 丙 | 1 | 0.5 | 1 | Q3 |
A.在上述条件下反应生成1mol SO3固体放热
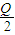 kJ
kJB.2Q3<2Q2=Q1<Q
C.Q1=2Q2=2Q3=Q
D.2Q2=2Q3<Q1<Q
某研究性学习小组对铝热反应实验展开研究.某高中化学教材中对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”、“纸漏斗的下部被烧穿,有熔融物落入沙中”.查阅《化学手册》知,Al、Al2O3、Fe、Fe2O3熔点、沸点数据如下:
Ⅰ.(1)某同学推测,铝热反应所得到的熔融物应是铁铝合金.理由是:该反应放出的热量使铁熔化,而铝的溶点比铁低,此时液态的铁和铝熔合形成铁铝合金.你认为他的解释是否合理?答 (填“合理”或“不合理”)
(2)设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝.该实验所用试剂是 ,反应的离子方程式为 .
(3)实验室溶解该熔融物,在下列试剂中最适宜的试剂是 (填序号).
A.浓硫酸B.稀硫酸C.稀硝酸D.氢氧化钠溶液
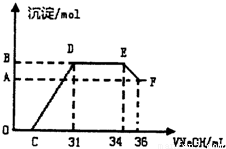
Ⅱ.实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低.某同学取一定量上这的熔融物与一定量很稀的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入4mol?L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如右图所示,试回答下列问题:
(1)图中OC段没有沉淀生成,此阶段发生反应的离子方程式为 .
(2)在DE段,沉淀的物质的最没有变化,则此阶段发生反应的离子方程式为 ,上述现象说明溶液中的离子结合OH-的能力最强的是 最弱的是 (填离子符号)
(3)B与A的差值为 mol.
0 62860 62868 62874 62878 62884 62886 62890 62896 62898 62904 62910 62914 62916 62920 62926 62928 62934 62938 62940 62944 62946 62950 62952 62954 62955 62956 62958 62959 62960 62962 62964 62968 62970 62974 62976 62980 62986 62988 62994 62998 63000 63004 63010 63016 63018 63024 63028 63030 63036 63040 63046 63054 203614
| 物质 | Al | Al2O3 | Fe | Fe2O3 |
| 熔点/℃ | 660 | 2054 | 1535 | 1462 |
| 沸点/℃ | 2467 | 2980 | 2750 | - |
(2)设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝.该实验所用试剂是 ,反应的离子方程式为 .
(3)实验室溶解该熔融物,在下列试剂中最适宜的试剂是 (填序号).
A.浓硫酸B.稀硫酸C.稀硝酸D.氢氧化钠溶液
Ⅱ.实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低.某同学取一定量上这的熔融物与一定量很稀的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入4mol?L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如右图所示,试回答下列问题:
(1)图中OC段没有沉淀生成,此阶段发生反应的离子方程式为 .
(2)在DE段,沉淀的物质的最没有变化,则此阶段发生反应的离子方程式为 ,上述现象说明溶液中的离子结合OH-的能力最强的是 最弱的是 (填离子符号)
(3)B与A的差值为 mol.