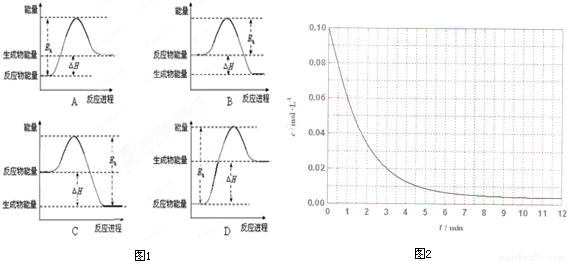
A、B、C三种强电解质,它们在水中电离出的离子如下表所示:
图1所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的A溶液、足量的B溶液、足量的C溶液,电极均为石墨电极.
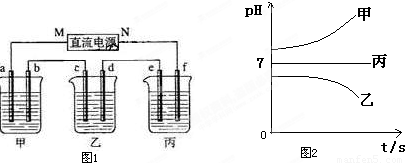
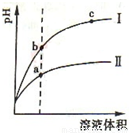
接通电源,经过一段时间后,测得乙中c电极质量增加了16g.常温下各烧杯中溶液的pH与电解时间t的关系图如图2.据此回答下列问题:
(1)M为电源的 极(填写“正”或“负”);电极b上发生的电极反应为 ;
(2)写出乙烧杯的电解反应方程式 ;
(3)计算电极e上生成的气体在标准状态下的体积 ;
(4)要使丙恢复到原来的状态,需要加入一种 物质 克.
| 阳离子 | Na+、K+、Cu2+ |
| 阴离子 | SO42-、OH- |

接通电源,经过一段时间后,测得乙中c电极质量增加了16g.常温下各烧杯中溶液的pH与电解时间t的关系图如图2.据此回答下列问题:
(1)M为电源的 极(填写“正”或“负”);电极b上发生的电极反应为 ;
(2)写出乙烧杯的电解反应方程式 ;
(3)计算电极e上生成的气体在标准状态下的体积 ;
(4)要使丙恢复到原来的状态,需要加入一种 物质 克.
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
①将碱式滴定管用蒸馏水洗净后,用待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放入20.00mL待测溶液到锥形瓶中.
②将酸式滴定管用蒸馏水洗净后,立即向其中注入0.1000mol?L-1标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数.
③向锥形瓶中滴入酚酞作指示剂,进行滴定.滴定至指示剂刚好变色,且半分钟内颜色不再改变为止,测得所耗盐酸的体积为V1mL.
④重复以上过程,但在滴定过程中向锥形瓶加入5mL的蒸馏水,测得所耗盐酸的体积为V2mL.
试回答下列问题:
(1)锥形瓶的溶液从 色变为 色时,停止滴定;
(2)滴定时边滴边摇动锥形瓶,眼睛观察 (填序号)
a.滴定管内液面的变化b.锥形瓶内溶液颜色的变化
(3)步骤①中错误的操作时 (请指出具体的错误).由此造成的测定结果是 (填偏高、偏低或无影响);
(4)②缺少的操作是 ;
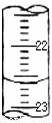
(5)某次滴定时的滴定管中的液面如图,其读数为 ml.
(6)根据下列数据:
请计算待测NaOH溶液的浓度为 mol?L-1.
0 62767 62775 62781 62785 62791 62793 62797 62803 62805 62811 62817 62821 62823 62827 62833 62835 62841 62845 62847 62851 62853 62857 62859 62861 62862 62863 62865 62866 62867 62869 62871 62875 62877 62881 62883 62887 62893 62895 62901 62905 62907 62911 62917 62923 62925 62931 62935 62937 62943 62947 62953 62961 203614
①将碱式滴定管用蒸馏水洗净后,用待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放入20.00mL待测溶液到锥形瓶中.
②将酸式滴定管用蒸馏水洗净后,立即向其中注入0.1000mol?L-1标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数.
③向锥形瓶中滴入酚酞作指示剂,进行滴定.滴定至指示剂刚好变色,且半分钟内颜色不再改变为止,测得所耗盐酸的体积为V1mL.
④重复以上过程,但在滴定过程中向锥形瓶加入5mL的蒸馏水,测得所耗盐酸的体积为V2mL.
试回答下列问题:
(1)锥形瓶的溶液从 色变为 色时,停止滴定;
(2)滴定时边滴边摇动锥形瓶,眼睛观察 (填序号)
a.滴定管内液面的变化b.锥形瓶内溶液颜色的变化
(3)步骤①中错误的操作时 (请指出具体的错误).由此造成的测定结果是 (填偏高、偏低或无影响);
(4)②缺少的操作是 ;
(5)某次滴定时的滴定管中的液面如图,其读数为 ml.
(6)根据下列数据:
| 滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 20.00 | 0.50 | 25.40 |
| 第二次 | 20.00 | 4.00 | 29.10 |

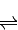 H++CH3COO-,下列叙述不正确的( )
H++CH3COO-,下列叙述不正确的( )
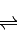 2SO3(g)△H=-196.6kJ?mol-1
2SO3(g)△H=-196.6kJ?mol-1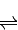 2NO2(g)△H=-113.0kJ?mol-1
2NO2(g)△H=-113.0kJ?mol-1 SO3(g)+NO(g)的△H= kJ?mol-1.
SO3(g)+NO(g)的△H= kJ?mol-1.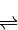 CH3OH(g).
CH3OH(g).