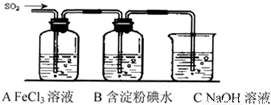
三氧化二铁和氧化亚铜都是红色粉末,常用作颜料.某校化学实验小组通过实验探究某红色粉末是Fe2O3、Cu2O或二者混合物.探究过程如下:
查阅资料:Cu2O是一种碱性氧化物,溶于稀硫酸生成Cu和CuSO4.
设计探究实验:取少量粉末放入足量稀硫酸中,在所得溶液中滴加KSCN试剂.
(1)若只有Fe2O3,则实验现象是 .
(2)若固体粉末完全溶解无固体存在,滴加KSCN试剂时溶液不变红色,则此过程中的离子反应为: .
(3)经实验分析,确定红色粉末为Cu2O和Fe2O3的混合物.实验小组欲测定Cu2O的质量分数.已知Cu2O在空气中加热生成CuO.
测定流程:
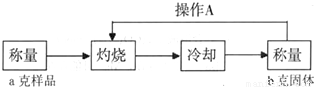
实验中操作A的名称为 .
灼烧过程中,所需仪器有:酒精灯、玻璃棒、 等(夹持仪器除外).
(4)写出混合物中Cu2O的质量分数的表达式 .
实验小组欲利用红色粉末制取较纯净的胆矾.经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如下:
实验室有下列试剂可供选择:A.氯水 B.H2O2 C.NaOH D.Cu2(OH)2CO3
实验小组设计如下实验方案制取胆矾:
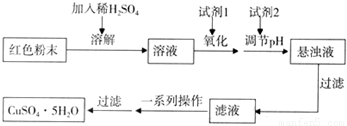
(5)用试剂编号表示:试剂l为 ,试剂2为 .
(6)为什么先“氧化”后“调节pH”?pH控制范围为多少? .
0 62617 62625 62631 62635 62641 62643 62647 62653 62655 62661 62667 62671 62673 62677 62683 62685 62691 62695 62697 62701 62703 62707 62709 62711 62712 62713 62715 62716 62717 62719 62721 62725 62727 62731 62733 62737 62743 62745 62751 62755 62757 62761 62767 62773 62775 62781 62785 62787 62793 62797 62803 62811 203614
查阅资料:Cu2O是一种碱性氧化物,溶于稀硫酸生成Cu和CuSO4.
设计探究实验:取少量粉末放入足量稀硫酸中,在所得溶液中滴加KSCN试剂.
(1)若只有Fe2O3,则实验现象是 .
(2)若固体粉末完全溶解无固体存在,滴加KSCN试剂时溶液不变红色,则此过程中的离子反应为: .
(3)经实验分析,确定红色粉末为Cu2O和Fe2O3的混合物.实验小组欲测定Cu2O的质量分数.已知Cu2O在空气中加热生成CuO.
测定流程:

实验中操作A的名称为 .
灼烧过程中,所需仪器有:酒精灯、玻璃棒、 等(夹持仪器除外).
(4)写出混合物中Cu2O的质量分数的表达式 .
实验小组欲利用红色粉末制取较纯净的胆矾.经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如下:
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 6.0 | 7.5 | 1.4 |
| 沉淀完全pH | 13 | 14 | 3.7 |
实验小组设计如下实验方案制取胆矾:

(5)用试剂编号表示:试剂l为 ,试剂2为 .
(6)为什么先“氧化”后“调节pH”?pH控制范围为多少? .

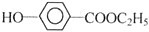 ),(俗称尼泊金乙酯)可用作防腐剂,对霉菌有很强的抑制作用.其过程如下:
),(俗称尼泊金乙酯)可用作防腐剂,对霉菌有很强的抑制作用.其过程如下: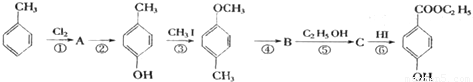
 CO↑+H2↑.甲酸苯丙酯(F)是生产香料和药物的主要原料.下图是用煤为原料合成甲酸苯丙酯的路线图(部分反应条件和生成物已略去)其中D的分子式为C9H10O,且能发生银镜反应.
CO↑+H2↑.甲酸苯丙酯(F)是生产香料和药物的主要原料.下图是用煤为原料合成甲酸苯丙酯的路线图(部分反应条件和生成物已略去)其中D的分子式为C9H10O,且能发生银镜反应.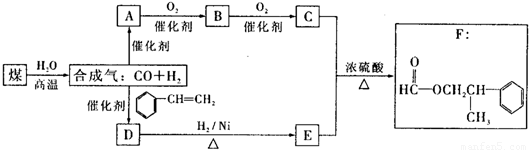
 4NO+6H2O,4NO+3O2+2H2O→4HNO3
4NO+6H2O,4NO+3O2+2H2O→4HNO3