已知复分解反应:2CH3COOH+Na2CO3═2CH3COONa+H2O+CO2↑可自发进行.在常温下,测得浓度均为0.1mol/L的下列六种溶液的PH:
表中数据提示出复分解反应的一条规律,即碱性较强的物质发生类似反应可生成碱性较弱的物质.依据该规律,请你判断下列反应不能成立的是( )
A.CO2+H2O+NaClO═NaHCO3+HClO
B.CO2+H2O+2NaClO═Na2CO3+2HClO
C.CH3COOH+NaCN═CH3COONa+HCN
D.CH3COOH+NaClO═CH3COONa+HClO
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH值 | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
A.CO2+H2O+NaClO═NaHCO3+HClO
B.CO2+H2O+2NaClO═Na2CO3+2HClO
C.CH3COOH+NaCN═CH3COONa+HCN
D.CH3COOH+NaClO═CH3COONa+HClO
化学在能源开发与利用中起到十分关键的作用.氢气是一种新型的绿色能源,又是一种重要的化工原料.
Ⅰ(1)在298K、101kPa时,2g H2完全燃烧生成液态水,放出285.8kJ热量.则表示氢气燃烧热的热化学方程式为:______.
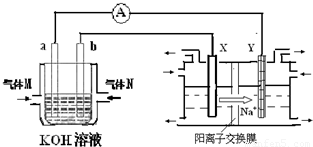
氢氧燃料电池能量转化率高,具有广阔的发展前景.现用氢氧燃料电池进行下图饱和食盐水电解实验(图中所用电极均为惰性电极).分析该装置、回答下列问题:
(2)氢氧燃料电池中,a电极为电池的是______(填“正极”或“负极”),气体M的分子式______,a电极上发生的电极反应式为:______.
(3)若右上图装置中盛有100mL5.0mol/LNaCl溶液,电解一段时间后须加入10.0mol/L盐酸溶液50mL(密度为1.02g/mL)才能使溶液恢复至原来状态.则在此电解过程中导线上转移的电子数为______mol.(保留小数点后2位)
Ⅱ氢气是合成氨的重要原料.工业上合成氨的反应是:
N2(g)+3H2(g)?2NH3 (g)△H=-92.2kJ?mol-1
(4)下列事实中,不能说明上述可逆反应已经达到平衡的是______.
①N2、H2、NH3的体积分数不再改变;
②单位时间内生成2n mol NH3的同时生成3n mol H2;
③单位时间内生成3n mol N-H键的同时生成n mol N≡N;
④用N2、H2、NH3的物质的量浓度变化表示的反应速率之比为1:3:2;
⑤混合气体的平均摩尔质量不再改变;
⑥混合气体的总物质的量不再改变.
(5)已知合成氨反应在某温度下2.00L的密闭容器中反应,测得如下数据:
根据表中数据计算:
①反应进行到2小时时放出的热量为______kJ.
②0~1小时内N2的平均反应速率______mol?L-1?h-1.
③此条件下该反应的化学平衡常数K═______(保留两位小数).
④反应达到平衡后,若往平衡体系中再加入N2、H2 和NH3各1mol,化学平衡向______方向移动(填“正反应”或“逆反应”或“不移动”.)
Ⅰ(1)在298K、101kPa时,2g H2完全燃烧生成液态水,放出285.8kJ热量.则表示氢气燃烧热的热化学方程式为:______.
氢氧燃料电池能量转化率高,具有广阔的发展前景.现用氢氧燃料电池进行下图饱和食盐水电解实验(图中所用电极均为惰性电极).分析该装置、回答下列问题:
(2)氢氧燃料电池中,a电极为电池的是______(填“正极”或“负极”),气体M的分子式______,a电极上发生的电极反应式为:______.
(3)若右上图装置中盛有100mL5.0mol/LNaCl溶液,电解一段时间后须加入10.0mol/L盐酸溶液50mL(密度为1.02g/mL)才能使溶液恢复至原来状态.则在此电解过程中导线上转移的电子数为______mol.(保留小数点后2位)
Ⅱ氢气是合成氨的重要原料.工业上合成氨的反应是:
N2(g)+3H2(g)?2NH3 (g)△H=-92.2kJ?mol-1
(4)下列事实中,不能说明上述可逆反应已经达到平衡的是______.
①N2、H2、NH3的体积分数不再改变;
②单位时间内生成2n mol NH3的同时生成3n mol H2;
③单位时间内生成3n mol N-H键的同时生成n mol N≡N;
④用N2、H2、NH3的物质的量浓度变化表示的反应速率之比为1:3:2;
⑤混合气体的平均摩尔质量不再改变;
⑥混合气体的总物质的量不再改变.
(5)已知合成氨反应在某温度下2.00L的密闭容器中反应,测得如下数据:
| 物质的量/(mol)/时间(h) | 1 | 2 | 3 | 4 | |
| N2 | 1.50 | n1 | 1.20 | n3 | 1.00 |
| H2 | 4.50 | 4.20 | 3.60 | n4 | 3.00 |
| NH3 | 0.00 | 0.20 | n2 | 1.00 | 1.00 |
①反应进行到2小时时放出的热量为______kJ.
②0~1小时内N2的平均反应速率______mol?L-1?h-1.
③此条件下该反应的化学平衡常数K═______(保留两位小数).
④反应达到平衡后,若往平衡体系中再加入N2、H2 和NH3各1mol,化学平衡向______方向移动(填“正反应”或“逆反应”或“不移动”.)

为测定含有Na2O杂质的Na2O2样品的纯度,甲、乙二位同学设计了二种不同的实验方案.
已知:2Na2O2+2CO2═2Na2CO3+O2
2Na2O2+2H2O═4NaOH+O2
甲:用图l所示装置,通过测定Na2O2与CO2反应生成O2的体积来测定样品的纯度.
(1)C中所盛的药品是:______.
(2)A中橡皮管的作用是:______.
(3)利用该实验方案所测Na2O2的纯度明显偏大,其原因可能是______(填选项字母).
a.装置A、B中的空气对测定结果产生了影响
b.装置C中的空气对测定结果产生了影响
c.读数时U形量气管中的液面左高右低
d.读数时U形量气管中的液面左低右高
乙:称取3.500g试样,配成1000.00mL溶液,用0.1000mol?L-1的标准盐酸滴定.
(4)取上述所配溶液25.00mL于锥形瓶中,操作如下图所示(手持部分省略):正确的操作是图______,取溶液所用仪器的名称是______.

(5)滴定操作平行实验的数据记录如下表:
由表中数据计算样品中Na2O2纯度为______.

0 62574 62582 62588 62592 62598 62600 62604 62610 62612 62618 62624 62628 62630 62634 62640 62642 62648 62652 62654 62658 62660 62664 62666 62668 62669 62670 62672 62673 62674 62676 62678 62682 62684 62688 62690 62694 62700 62702 62708 62712 62714 62718 62724 62730 62732 62738 62742 62744 62750 62754 62760 62768 203614
已知:2Na2O2+2CO2═2Na2CO3+O2
2Na2O2+2H2O═4NaOH+O2
甲:用图l所示装置,通过测定Na2O2与CO2反应生成O2的体积来测定样品的纯度.
(1)C中所盛的药品是:______.
(2)A中橡皮管的作用是:______.
(3)利用该实验方案所测Na2O2的纯度明显偏大,其原因可能是______(填选项字母).
a.装置A、B中的空气对测定结果产生了影响
b.装置C中的空气对测定结果产生了影响
c.读数时U形量气管中的液面左高右低
d.读数时U形量气管中的液面左低右高
乙:称取3.500g试样,配成1000.00mL溶液,用0.1000mol?L-1的标准盐酸滴定.
(4)取上述所配溶液25.00mL于锥形瓶中,操作如下图所示(手持部分省略):正确的操作是图______,取溶液所用仪器的名称是______.

(5)滴定操作平行实验的数据记录如下表:
| 滴定次数 | 第一次滴定 | 第二次滴定 | 第三次滴定 |
| 消耗标准盐酸的体积(mL) | 24.98 | 25.00 | 25.02 |

 -O-+CO2+H2O→2
-O-+CO2+H2O→2 -OH+CO32-
-OH+CO32- 乙+丙
乙+丙  氧化物+H2O
氧化物+H2O