实验室可用铝屑、氨水、氢氧化钠溶液、稀硫酸等来制备氢氧化铝,某同学设计了三种方案,
(1)用方案 ①制备Al(OH)3时使用的药品最好是铝屑、稀硫酸和氨水,不用氢氧化钠代替氨水的原因是______;写出该方案中有关的离子方程式:______.
(2)用方案 ②来制备Al(OH)3时,必须注意______ 的用量,以防止生成的Al(OH)3溶解.
(3)完成下表
三种方案中,你认为最好的是______ (填序号),原因是______.
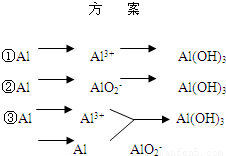
(1)用方案 ①制备Al(OH)3时使用的药品最好是铝屑、稀硫酸和氨水,不用氢氧化钠代替氨水的原因是______;写出该方案中有关的离子方程式:______.
(2)用方案 ②来制备Al(OH)3时,必须注意______ 的用量,以防止生成的Al(OH)3溶解.
(3)完成下表
| 方 案 | 生成1mol Al(OH)3消耗H+ 或 OH- 的物质的量/mol | |
| 消耗H+ | 消耗OH- | |
| ① | 3 | ______ |
| ② | ______ | 1 |
| ③ | 3/4 | ______ |

硫酸是工业生产中一种重要的化工产品,我国工业生产硫酸的主要方法是接触法,主要原料为黄铁矿,请回答下列问题:
(1)已知煅烧黄铁矿的化学方程式为 4FeS2+11O2 2Fe2O3+8SO2;该反应中氧化剂和氧化产物的物质的量之比为______;标准状态下得到4.48升SO2时,一共转移了______mole-.
2Fe2O3+8SO2;该反应中氧化剂和氧化产物的物质的量之比为______;标准状态下得到4.48升SO2时,一共转移了______mole-.
(2)已知温度、压强对SO2平衡转化率的影响如下表所示:
根据上表回答,SO2转化到SO3的最佳反应条件是______.
A.400-500℃0.1MPa B.400℃10MPa
C.500℃10MPa D.400-500℃1MPa
(3)在一定条件下,1mol SO2完全转化成SO3气体时放出热量为Q1 KJ,写出该反应的热化学方程式:______.若在该条件下将2mol SO2 放入一定容积的密闭容器中,一段时间后测得反应放出热量为Q2 KJ,则此时SO2的转化率为______ (用含Q1、Q2代数式表示).
(4)市售浓硫酸的密度是1.84g/cm3、质量分数为98%,若用H2SO4?XH2O来表示这种浓硫酸,则X为______.
0 62538 62546 62552 62556 62562 62564 62568 62574 62576 62582 62588 62592 62594 62598 62604 62606 62612 62616 62618 62622 62624 62628 62630 62632 62633 62634 62636 62637 62638 62640 62642 62646 62648 62652 62654 62658 62664 62666 62672 62676 62678 62682 62688 62694 62696 62702 62706 62708 62714 62718 62724 62732 203614
(1)已知煅烧黄铁矿的化学方程式为 4FeS2+11O2
 2Fe2O3+8SO2;该反应中氧化剂和氧化产物的物质的量之比为______;标准状态下得到4.48升SO2时,一共转移了______mole-.
2Fe2O3+8SO2;该反应中氧化剂和氧化产物的物质的量之比为______;标准状态下得到4.48升SO2时,一共转移了______mole-.(2)已知温度、压强对SO2平衡转化率的影响如下表所示:
压强/MPa 转化率/% 温度/℃ | 0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
A.400-500℃0.1MPa B.400℃10MPa
C.500℃10MPa D.400-500℃1MPa
(3)在一定条件下,1mol SO2完全转化成SO3气体时放出热量为Q1 KJ,写出该反应的热化学方程式:______.若在该条件下将2mol SO2 放入一定容积的密闭容器中,一段时间后测得反应放出热量为Q2 KJ,则此时SO2的转化率为______ (用含Q1、Q2代数式表示).
(4)市售浓硫酸的密度是1.84g/cm3、质量分数为98%,若用H2SO4?XH2O来表示这种浓硫酸,则X为______.
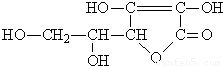 ,有关它的叙述正确的是( )
,有关它的叙述正确的是( ) W(g)+Z(g)(正反应是放热反应),在一体积不变的容器中反应达到平衡后,改变条件,反应速率(v)随时间变化的情况如下图所示:下列条件的改变与图中情况相符的是( )
W(g)+Z(g)(正反应是放热反应),在一体积不变的容器中反应达到平衡后,改变条件,反应速率(v)随时间变化的情况如下图所示:下列条件的改变与图中情况相符的是( )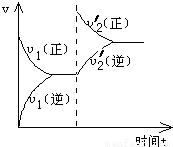

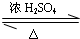 Z+H2O;写出该反应的化学方程式______,反应类型为______.
Z+H2O;写出该反应的化学方程式______,反应类型为______.