下列物质的分类正确的是( )
A.A
B.B
C.C
D.D
| 碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 | |
| A | Na2CO3 | H2SO4 | NaOH | SO2 | CO2 |
| B | NaOH | HCl | NaCl | Na2O | CO |
| C | NaOH | CH3COOH | CaF2 | CO | SO2 |
| D | KOH | HNO3 | CaCO3 | CaO | SO2 |
A.A
B.B
C.C
D.D
下列五组物质分离所涉及的实例、性质差异和分离方法的组合正确的是( )
A.①a和③c丙
B.②b乙和⑤e戊
C.④d丁和⑤e戊
D.①a和④d丁
| 实 例 | 物质性质差异 | 分离方法 |
| ①除去氯化钠溶液中的泥沙 | a在水中溶解度的差异 | 甲 蒸馏 |
| ②用四氯化碳提取溴水中的溴单质 | b在不同溶剂中溶解度的差异 | 乙 萃取 |
| ③分离乙酸(沸点118°C)与乙酸乙酯(沸点77.1°C) | c沸点的差异 | 丙 分液 |
| ④分离汽油和水 | d互不相溶 | 丁 过滤 |
| ⑤从含少量氯化钠的硝酸钾溶液中提取硝酸钾 | e溶解度随温度变化的差异 | 戊 结晶 |
A.①a和③c丙
B.②b乙和⑤e戊
C.④d丁和⑤e戊
D.①a和④d丁
漂白粉是一种常用杀菌、消毒剂,其有效成分为次氯酸钙.下图为制取漂白粉的工业流程简图.
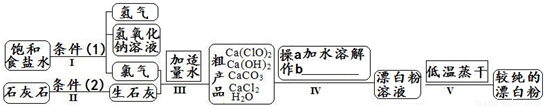
(1)流程I 得到浓度为80g?L-1氢氧化钠溶液,其物质的量浓度是______ mol?L-1.
(2)写出流程I发生反应的化学反应方程式,并用双线桥表示其电子转移的方向和数目:______.流程II的反应条件(2)是______.
(3)流程III中发生两个反应,写出其中的氧化还原反应的化学反应方程______.其中氧化剂是______;还原剂是______.(写化学式)
(4)流程IV中操作b是:______.(写名称)
(5)流程V进行低温蒸干的原因是:______.
(6)用化学方程式说明较纯的次氯酸钙粉末必须密封保存的原因______.
(7)氯水和次氯酸钙都能起漂白、消毒作用.是因为它们都能产生同一种物质,写出氯气与水反应产生该物质的化学方程式______.
(8)在酸性条件下次氯酸钙的氧化性比氯气强,能将溴离子氧化成溴单质,而次氯酸钙中的氯元素则被还原为负一价的氯离子,氧元素则转化为水.试写出次氯酸钙和稀盐酸的混合物与溴化钠反应的化学方程式:______.
0 62303 62311 62317 62321 62327 62329 62333 62339 62341 62347 62353 62357 62359 62363 62369 62371 62377 62381 62383 62387 62389 62393 62395 62397 62398 62399 62401 62402 62403 62405 62407 62411 62413 62417 62419 62423 62429 62431 62437 62441 62443 62447 62453 62459 62461 62467 62471 62473 62479 62483 62489 62497 203614
| 信息卡 常温下碳酸钙难溶于水,氢氧化钙微溶于水,氯化钙易溶于水.次氯酸钙易溶于水,酸性条件下不稳定、100°C时发生分解反应. |

(1)流程I 得到浓度为80g?L-1氢氧化钠溶液,其物质的量浓度是______ mol?L-1.
(2)写出流程I发生反应的化学反应方程式,并用双线桥表示其电子转移的方向和数目:______.流程II的反应条件(2)是______.
(3)流程III中发生两个反应,写出其中的氧化还原反应的化学反应方程______.其中氧化剂是______;还原剂是______.(写化学式)
(4)流程IV中操作b是:______.(写名称)
(5)流程V进行低温蒸干的原因是:______.
(6)用化学方程式说明较纯的次氯酸钙粉末必须密封保存的原因______.
(7)氯水和次氯酸钙都能起漂白、消毒作用.是因为它们都能产生同一种物质,写出氯气与水反应产生该物质的化学方程式______.
(8)在酸性条件下次氯酸钙的氧化性比氯气强,能将溴离子氧化成溴单质,而次氯酸钙中的氯元素则被还原为负一价的氯离子,氧元素则转化为水.试写出次氯酸钙和稀盐酸的混合物与溴化钠反应的化学方程式:______.

 MnCl2+Cl2↑+2H2O 若取含0.8molHCl溶质的浓盐酸和足量二氧化锰共热,则得到的氯气换算成标准状况下的体积为( )
MnCl2+Cl2↑+2H2O 若取含0.8molHCl溶质的浓盐酸和足量二氧化锰共热,则得到的氯气换算成标准状况下的体积为( )