某温度时,在2L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如表所示.

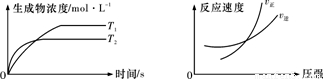
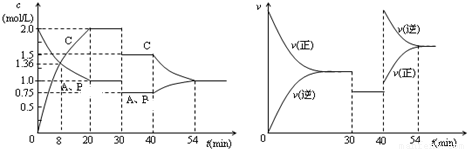
(1)根据左表中数据,在图1中画出X、Y、Z的物质的量(n)随时间(t)变化的曲线:______
(2)体系中发生反应的化学方程式是______;
(3)列式计算该反应在0-3min时间内产物Z的平均反应速率:______;
(4)该反应达到平衡时反应物X的转化率α等于______;
(5)如果该反应是放热反应.改变实验条件(温度、压强、催化剂)得到Z随时间变化的曲线①、②、③(如图2所示)则曲线①、②、③所对应的实验条件改变分别是:①______ ②______ ③______.
| t/min | X/mol | Y/mol | Z/mol |
| 1.00 | 1.00 | 0.00 | |
| 1 | 0.90 | 0.80 | 0.20 |
| 3 | 0.75 | 0.50 | 0.50 |
| 5 | 0.65 | 0.30 | 0.70 |
| 9 | 0.55 | 0.10 | 0.90 |
| 10 | 0.55 | 0.10 | 0.90 |
| 14 | 0.55 | 0.10 | 0.90 |

(1)根据左表中数据,在图1中画出X、Y、Z的物质的量(n)随时间(t)变化的曲线:______
(2)体系中发生反应的化学方程式是______;
(3)列式计算该反应在0-3min时间内产物Z的平均反应速率:______;
(4)该反应达到平衡时反应物X的转化率α等于______;
(5)如果该反应是放热反应.改变实验条件(温度、压强、催化剂)得到Z随时间变化的曲线①、②、③(如图2所示)则曲线①、②、③所对应的实验条件改变分别是:①______ ②______ ③______.
二甲醚是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用.工业上可利用煤的气化产物(水煤气)合成二甲醚(CH3OCH3).
请回答下列问题:
(1)煤的气化过程中产生的有害气体H2S用Na2CO3溶液吸收,生成两种酸式盐,该反应的化学方程式为:______
(2)利用水煤气合成二甲醚的三步反应如下:
①2H2(g)+CO(g)?CH3OH(g)△H=-90.8kJ?mol-1
②2CH3OH(g)?CH3OCH3(g)+H2O(g)△H=-23.5kJ?mol-1
③CO(g)+H2O(g)?CO2(g)+H2(g)△H=-41.3kJ?mol-1
总反应:3H2(g)+3CO(g)?CH3OCH3(g)+CO2(g)的△H=______
一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是:______(填字母代号).
a.压缩体积 b.加入催化剂 c.减少CO2的浓度
d.增加CO的浓度 e.分离出二甲醚(CH3OCH3)
(3)已知反应②:2CH3OH(g)?CH3OCH3(g)+H2O(g)△H=-23.5kJ?mol-1
某温度下的平衡常数为400.此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
①比较此时正、逆反应速率的大小比较:v正______ v逆 (填“>”、“<”或“=”).
②该反应的平衡常数的表达式为K=______ 温度升高,该反应的平衡常数K______(填“增大”、“减小”或“不变”).
0 62166 62174 62180 62184 62190 62192 62196 62202 62204 62210 62216 62220 62222 62226 62232 62234 62240 62244 62246 62250 62252 62256 62258 62260 62261 62262 62264 62265 62266 62268 62270 62274 62276 62280 62282 62286 62292 62294 62300 62304 62306 62310 62316 62322 62324 62330 62334 62336 62342 62346 62352 62360 203614
请回答下列问题:
(1)煤的气化过程中产生的有害气体H2S用Na2CO3溶液吸收,生成两种酸式盐,该反应的化学方程式为:______
(2)利用水煤气合成二甲醚的三步反应如下:
①2H2(g)+CO(g)?CH3OH(g)△H=-90.8kJ?mol-1
②2CH3OH(g)?CH3OCH3(g)+H2O(g)△H=-23.5kJ?mol-1
③CO(g)+H2O(g)?CO2(g)+H2(g)△H=-41.3kJ?mol-1
总反应:3H2(g)+3CO(g)?CH3OCH3(g)+CO2(g)的△H=______
一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是:______(填字母代号).
a.压缩体积 b.加入催化剂 c.减少CO2的浓度
d.增加CO的浓度 e.分离出二甲醚(CH3OCH3)
(3)已知反应②:2CH3OH(g)?CH3OCH3(g)+H2O(g)△H=-23.5kJ?mol-1
某温度下的平衡常数为400.此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度 | 0.40 | 0.6 | 0.6 |
②该反应的平衡常数的表达式为K=______ 温度升高,该反应的平衡常数K______(填“增大”、“减小”或“不变”).