0 62088 62096 62102 62106 62112 62114 62118 62124 62126 62132 62138 62142 62144 62148 62154 62156 62162 62166 62168 62172 62174 62178 62180 62182 62183 62184 62186 62187 62188 62190 62192 62196 62198 62202 62204 62208 62214 62216 62222 62226 62228 62232 62238 62244 62246 62252 62256 62258 62264 62268 62274 62282 203614
 CO(g)+3H2(g),试回答下列问题。
CO(g)+3H2(g),试回答下列问题。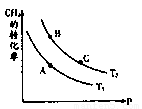


 Na2S4+3NaBr反应原理进行工作,电解质通过泵不断在储罐和电池间循环;电池中的左右两侧为电极,中间为离子选择性膜,在电池放电和充电时该膜可允许钠离子通过。
Na2S4+3NaBr反应原理进行工作,电解质通过泵不断在储罐和电池间循环;电池中的左右两侧为电极,中间为离子选择性膜,在电池放电和充电时该膜可允许钠离子通过。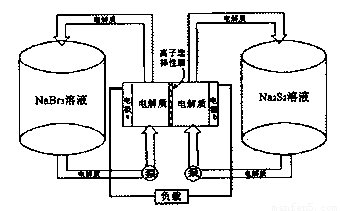

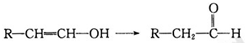 化学式为C11H10O4的有机物A有如下的转化关系
化学式为C11H10O4的有机物A有如下的转化关系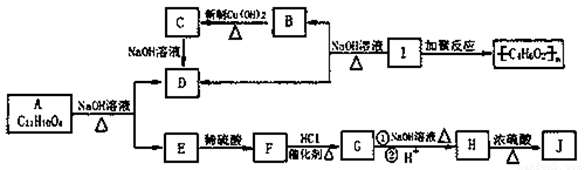
 2Ni(OH)2。根据此反应式,下列 有关说法中正确的是:
2Ni(OH)2。根据此反应式,下列 有关说法中正确的是:  H++CH3COO-,下列叙述不正确的是
H++CH3COO-,下列叙述不正确的是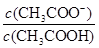 不变
不变 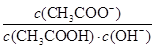 不变
不变 R-O-R(醚)+H2O,分子式为C2H6O和C3H8O醇的混合物在一定条件下脱水形成的醚最多有
R-O-R(醚)+H2O,分子式为C2H6O和C3H8O醇的混合物在一定条件下脱水形成的醚最多有