废易拉罐的成分比较复杂,据查,铝易拉罐各部分成分及含量(质量百分含量)见表:
|
|
Si |
Fe |
Cu |
Mn |
Mg |
Cr |
Zn |
Ti |
Al |
|
罐身/% |
0.3 |
0.7 |
0.25 |
0.25 |
1.0~1.5 |
|
|
|
其余 |
|
罐盖/% |
0.2 |
0.35 |
0.15 |
0.2~0.5 |
4.0~5.0 |
|
0.1 |
0.25 |
其余 |
|
拉环/% |
0.2 |
0.35 |
0.15 |
0.2~0.5 |
3.0~4.0 |
0.1 |
0.25 |
0.1 |
其余 |
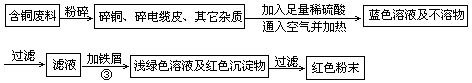
为了验证罐身的组成成分,进行了如下实验:
【实验仪器与药品】
仪器:酒精灯、烧杯、试管、试管夹、漏斗、滤纸、铁圈、玻璃棒、砂纸、剪刀
药品:易拉罐、去污粉、NaOH溶液、KSCN溶液、盐酸、镁试剂、高碘酸(H3IO6,弱酸)
【实验方案】
实验预处理:将剪好的易拉罐片用砂纸打磨,除去表面的涂料层,直到光亮后用去污粉清洗干净备用。
【实验过程】分别向试管a、b中加入少量上述易拉罐片,进行如下操作:

请填写下列空白:
(1)图中操作①②所用到的玻璃仪器有 。
(2)沉淀A的成分为 。
(3)操作③观察到的现象为 ;反应的离子方程式为 、
、 。
(4)若试管a、b中取样相同,则分别加入足量的NaOH溶液、稀盐酸后,相同条件下理论上产生的气体体积V(a) V(b)(填“>”、“<”或“=”)




 的邻位异构体分子内脱水产物香豆素的结构简式。
的邻位异构体分子内脱水产物香豆素的结构简式。 )的原料,写出检验A已完全转化为环己醇的方法。
)的原料,写出检验A已完全转化为环己醇的方法。
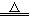 2CuSO4+2H2O
) ,于是他提出了另一套方案:
2CuSO4+2H2O
) ,于是他提出了另一套方案: