0 61865 61873 61879 61883 61889 61891 61895 61901 61903 61909 61915 61919 61921 61925 61931 61933 61939 61943 61945 61949 61951 61955 61957 61959 61960 61961 61963 61964 61965 61967 61969 61973 61975 61979 61981 61985 61991 61993 61999 62003 62005 62009 62015 62021 62023 62029 62033 62035 62041 62045 62051 62059 203614
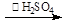
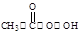 (过氧乙酸)+H2O
(过氧乙酸)+H2O ZnFe2(C2O4)3·6H2O↓……………(a)
ZnFe2(C2O4)3·6H2O↓……………(a) ZnFe2O4+2CO2↑+4CO↑+6H2O
……………(b)
ZnFe2O4+2CO2↑+4CO↑+6H2O
……………(b)






 的名称:2-甲基丁烷
的名称:2-甲基丁烷