温度为T时,向2.0 L恒容密闭容器中充入1.0 mol PCl5,反应PCl5(g) →PCl3(g)+Cl2(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表:
|
t/s |
0 |
50 |
150 |
250 |
350 |
|
n(PCl3)/mol |
0 |
0.16 |
0.19 |
0.20 |
0.20 |
下列说法正确的是
A.反应在前50 s内的平均速率v(PCl3)=0.0032 mol/(L·s)
B.保持其他条件不变,升高温度,平衡时c(PCl3)=0.11 mol·L-1,该反应为放热反应
C.相同温度下,起始时向容器中充入1.0 mol PCl5、0.20 mol PCl3和0.20 mol Cl2,达到平衡前v(正)>v(逆)
D.相同温度下,起始时向容器中充入 2.0 mol PCl3、2.0 mol Cl2,达到平衡时,PCl3的转化率小于80%
回答以下关于第三周期元素及其化合物的问题。
(1)下列能用于判断氧和氟非金属性强弱的是 (选填编号)。
A.气态氢化物的稳定性 B.最高价氧化物对应水化物的酸性
C.单质与氢气反应的难易 D.单质与同浓度酸发生反应的快慢
(2)Be和Al具有相似的化学性质,写出BeCl2水解反应的化学方程式
(3)常温下,不能与铝单质发生反应的是_________(填序号)
A.CuSO4溶液 B.Fe2O3 C.浓硫酸 D.NaOH E.Na2CO3固体
(4)相同压强下,部分元素氟化物的熔点见下表:
|
氟化物 |
NaF |
MgF2 |
SiF4 |
|
熔点/℃ |
1266 |
1534 |
183 |
试解释上表中氟化物熔点差异的原因: 。SiF4分子的空间构型为 ,SiF4中Si—F键间的键角 。(选填“相等”、“不相等”或“无法判断”)
(5)Cl2合成有机物时会产生副产物HC1。4HCl+O2 2Cl2+2H2O,可实现氯的循环利用。
2Cl2+2H2O,可实现氯的循环利用。
该反应平衡常数的表达式K= ;若反应容器的容积为2L,8min后达到平衡,测得容器内物质由2.5mol减少至2.25mol,则HCl的平均反应速率为 mol/L∙ min。
 不变
不变 4NH3
(g)+3O2 (g) - Q ,如果反应的平衡常数K值变大,该反应
(选填编号)。
4NH3
(g)+3O2 (g) - Q ,如果反应的平衡常数K值变大,该反应
(选填编号)。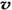 (N2)/
(N2)/ 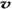 (O2)=2:3
(O2)=2:3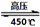 6H2O↑+
2N2↑+ 4HCl↑+ 5O2↑,其中氧化产物与还原产物的物质的量之比是
,每分解1mol高氯酸铵,转移的电子数目是
。
6H2O↑+
2N2↑+ 4HCl↑+ 5O2↑,其中氧化产物与还原产物的物质的量之比是
,每分解1mol高氯酸铵,转移的电子数目是
。

 CuY2–+
2H+。则CuSO4·5H2O质量分数的表达式是
。
CuY2–+
2H+。则CuSO4·5H2O质量分数的表达式是
。