一定条件下,向密闭容器中加入X物质发生反应:3X(g) 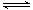 Y(g)
+ Z(g) △H<0,反应一段时间后改变某一个外界条件,反应中各时刻X物质的浓度如下表所示。下列说法中不正确的是
Y(g)
+ Z(g) △H<0,反应一段时间后改变某一个外界条件,反应中各时刻X物质的浓度如下表所示。下列说法中不正确的是
|
反应时间(min) |
0 |
5 |
15 |
17 |
20 |
|
X的浓度(mol·L-1) |
1.0 |
0.4 |
0.4 |
0.7 |
0.7 |
A.0~5 min时,该反应的速率为v(X)=0.12 mol·L-1·min-1
B.5 min时反应达到平衡,该温度下的平衡常数值为0.625
C.15 min时改变的条件可能是降低温度
D.从初始到18 min时,X的转化率为30 %
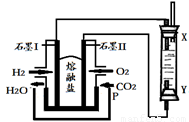
工业尾气中氮氧化物通常采用氨催化吸收法,其原理是NH3与NOx在催化剂作用下反应生成无毒的物质。某校活动小组同学采用以下装置和步骤模拟工业上氮氧化物的处理过程。

I.探究制取NH3的方法
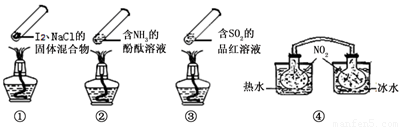
(1)在上述装置中,H能快速、简便制取NH3,装置中需要添加的反应试剂为 。
(2)为探究更好的实验效果,活动小组同学采用上述C装置来制取氨气,在控制实验条件相同的情况下,获得下表中实验数据。
|
试剂组合序号 |
固体试剂 |
NH3体积(mL) |
|
|
a |
6.0 g Ca(OH)2(过量) |
5.4 g NH4Cl |
1344 |
|
b |
5.4g (NH4)2SO4 |
1364 |
|
|
c |
6.0 g NaOH(过量) |
5.4 g NH4Cl |
1568 |
|
d |
5.4g (NH4)2SO4 |
1559 |
|
|
e |
6.0 g CaO(过量) |
5.4 g NH4Cl |
1753 |
|
f |
5.4 g (NH4)2SO4 |
1792 |
分析表中数据,你认为哪种方案制取氨气的效果最好 (填序号),从该方案选择的原料分析制气效果好的可能原因是 。
II.模拟尾气处理
活动小组同学选用上述部分装置,按下列顺序连接成模拟尾气处理装置进行实验。
(1)请从上述装置中选择你认为合理的进行补充(所选装置不能重复)。

(2)A中反应的离子方程式为 。
(3)D装置的作用有:使气体混合均匀、调节气流速度、 。
(4)D装置中的液体还可换成 (填序号)。
a.H2O b.CCl4 c.浓H2SO4 d.CuSO4溶液
(5)该小组同学所设计的模拟尾气处理装置中还存在一处明显的缺陷是 。
 Na2Mn5O10,请写出电池总反应式
。
Na2Mn5O10,请写出电池总反应式
。 O2(g)
O2(g) FeO(s)
△H=-272 kJ·mol-1
FeO(s)
△H=-272 kJ·mol-1  Fe(s)+CO2(g) △H=
。
Fe(s)+CO2(g) △H=
。