水解是物质与水发生反应形成新物质的反应.下列说法不正确的是( )
| A、Mg3N2的水解产物是两种碱 | B、CaC2的水解产物之一是C2H2 | C、PCl3的水解产物是HClO和PH3 | D、CaO2的水解产物是Ca(OH)2和H2O2 |
广义的水解观认为,无论是盐的水解还是非盐的水解,其最终结果都是反应中各物质和水分别解离成两部分,然后两两重新组合成新的物质.根据上述观点,下列说法错误的是( )
| A、(CH3)3COMgBr的水解产物是(CH3)3COH和Mg(OH)Br | B、ICl5的水解产物是HIO3和HClO | C、CaO2的水解产物是Ca(OH)2和H2O2 | D、A1(C2H5)3的水解产物是Al(OH)3与C2H6 |
下列溶液一定呈酸性的是( )
| A、pH=6的溶液 | B、含有H+的溶液 | C、遇酚酞显无色的溶液 | D、c(H+)>c(OH-)的溶液 |
下列说法中,正确的是( )
| A、用标准盐酸滴定待测氢氧化钠溶液浓度,水洗后的酸式滴定管未经标准液润洗,则滴定结果偏低 | B、配制0.1mol/L NaOH溶液时,用潮湿的烧杯称量NaOH固体,对配制结果无影响 | C、测定镀锌铁皮镀层厚度实验,当表面镀层反应完后需将铁皮用水洗,然后用酒精灯高温灼烧冷却后称量,以减少实验误差 | D、测定小苏打中Na2CO3含量的方案:取a(g)样品与足量稀硫酸充分反应,逸出的气体用碱石灰吸收,增重b(g) |
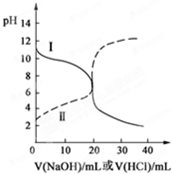 25℃时,取浓度均为0.1mol?L-1的醋酸溶液和氨水溶液各20mL,分别用0.1mol?L-1 NaOH溶液、0.1mol?L-1盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如图所示.下列说法正确的是( )
25℃时,取浓度均为0.1mol?L-1的醋酸溶液和氨水溶液各20mL,分别用0.1mol?L-1 NaOH溶液、0.1mol?L-1盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如图所示.下列说法正确的是( )| A、曲线Ⅰ:滴加溶液到10 mL时:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) | B、曲线Ⅰ:滴加溶液到20 mL时:c(Cl-)>c(NH4+)>c(OH-)>c(H+) | C、曲线Ⅱ:滴加溶液在10 mL~20 mL之间存在:c(NH4+)=c(Cl-)>c(OH-)=c(H+) | D、曲线Ⅱ:滴加溶液到10 mL时:c(CH3COO-)-c(CH3COOH)=2[c(H+)-c(OH-)] |
25℃时,用浓度为0.100mol/L的氢氧化钠溶液分别滴定20.00mL浓度均为0.100mol/L的二种酸HX、HY(忽略体积变化),实验数据如下表,下列判断正确的是( )
数据编号 |
NaOH加入的体积/mL |
溶液的pH | ||
| C(HX) | c(HY) | |||
| ① | 0 | 3 | 1 | |
| ② | a | 7 | ||
| ③ | 20.00 | x | y | |
| A、在相同温度下,同浓度的两种酸溶液的导电能力顺序HX<HY |
| B、由表中数据可估算出Ka(HX)≈10-5 |
| C、HY和HX混合,达到平衡时满足质子守恒 |
| D、上述②反应后的HY溶液中:c(Na+)>c(Y-)>c(OH-)>c(H+) |
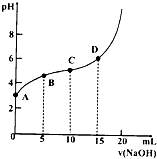 如图表示在20ml 0.1mol?L-1 CH3COOH溶液中逐滴加入0.1mo1?L-1的NaOH溶液的pH变化曲线.下列说法正确的是( )
如图表示在20ml 0.1mol?L-1 CH3COOH溶液中逐滴加入0.1mo1?L-1的NaOH溶液的pH变化曲线.下列说法正确的是( )A、A点溶液存在的关系:c(H+)=c(OH-)+Ka(CH3COOH)-
| ||
| B、C点溶液中各微粒浓度的大小关系为:c(CH3COOH)>c(CH3COO-)>c(Na+)>c(H+)>c(OH-) | ||
| C、在C点溶液中加少量的酸或碱溶液,pH变化不大 | ||
| D、D点为该反应的滴定终点 |
中和滴定实验中,下列说法正确的是( )
| A、滴定时视线必须注视滴定管中液面刻度的变化 | B、锥形瓶必须用待测液润洗 | C、滴定前必须使滴定管尖嘴部分充满液体 | D、滴定管不能用标准液润洗 |
用已知浓度的盐酸滴定未知浓度的NaOH溶液时,下列操作中正确的是( )
| A、酸式滴定管用蒸馏水洗净后,直接加入已知浓度的盐酸 | B、锥形瓶用蒸馏水洗净后,直接加入一定体积的未知浓度的NaOH溶液 | C、滴定时,没有逐出滴定管下口的气泡 | D、该实验中,某同学将消耗已知浓度的盐酸的体积记录为23.6mL |