在中和滴定实验中,不需要的仪器是( )
| A、滴定管 | B、锥形瓶 | C、烧杯 | D、胶头滴管 |
用0.1mol/L盐酸溶液滴定未知浓度的NaOH溶液时,在滴定开始酸式滴定管中液体读数时用平视,而在滴定达到终点酸式滴定管中液体读数时,用仰视.则待测液浓度会( )
| A、偏大 | B、偏小 | C、没有影响 | D、无法确定 |
用盐酸标准液来滴定NaOH待测液,下列操作可能会使测定结果偏低的是( )
| A、酸式滴定管只用水洗 | B、锥形瓶只用水洗 | C、使用甲基橙做指示剂 | D、观察酸式滴定管的刻度时仰视 |
下列有关说法中正确的是( )
| A、HCO3-水解:HCO3-+H2O?CO32-+H3O+ | B、中和滴定时眼睛必须注意锥形瓶内溶液颜色的变化 | C、电解水生成H2和O2的实验中,可加入少量盐酸或硫酸增强导电性 | D、用等浓度(0.5 mol?L-1)等体积(50 mL)的NaOH溶液与盐酸混合测定中和热 |
用已知浓度盐酸滴定未知浓度的NaOH溶液(装在锥形瓶内),下列操作使测定出的NaOH溶液浓度偏小的是( )
| A、锥形瓶用蒸馏水洗净后未烘干 | B、装盐酸的滴定管未润洗 | C、滴定管尖嘴处滴定前有一气泡,滴定后消失 | D、滴定管读数时,滴定前仰视读数,滴定后俯视读数 |
下列有关化学实验的叙述正确的是( )
| A、用待测液润洗滴定用的锥形瓶 | B、将pH试纸放入待测溶液中,测其pH | C、用稀盐酸洗涤盛放过石灰水的试剂瓶 | D、Na2CO3溶液保存在带玻璃塞的试剂瓶中 |
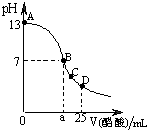 在25mL0.1mol/LNaOH溶液中逐滴加入0.2mol/L醋酸溶液,曲线如图所示,有关粒子浓度关系比较不正确的( )
在25mL0.1mol/LNaOH溶液中逐滴加入0.2mol/L醋酸溶液,曲线如图所示,有关粒子浓度关系比较不正确的( )| A、在A、B间任一点,溶液中一定都有c(Na+)>c(CH3COO-)>c(OH-)>c(H+) | B、在B点,a>12.5,且有c(Na+)=c(CH3COO-)=c(OH-)=c(H+) | C、在C点:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) | D、在D点:c(CH3COO-)+c(CH3COOH)=2c(Na+) |
关于图中各装置的叙述不正确的是( )
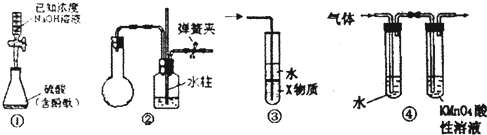

| A、装置①是中和滴定法测定硫酸的物质的量浓度 | B、装置②中手捂烧瓶(橡胶管已被弹簧夹夹紧),发现导管中有液柱上升并保持稳定,则说明装置不漏气 | C、装置③中X若为四氯化碳,可用于吸收氨气,并防止倒吸 | D、装置④可检验溴乙烷发生消去反应得到的气体中含有乙烯(假定每个装置中吸收完全) |
在含有Ag+的酸性溶液中,以铁铵矾NH4Fe(SO4)2作指示剂,用KSCN的标准溶液滴定Ag+.已知:
AgSCN(白色s)?Ag++SCN-,Ksp=1.0×10-12
Fe3++SCN-?FeSCN2+(红色),K=138
下列说法不正确的是( )
AgSCN(白色s)?Ag++SCN-,Ksp=1.0×10-12
Fe3++SCN-?FeSCN2+(红色),K=138
下列说法不正确的是( )
| A、边滴定,边摇动溶液,溶液中首先析出AgSCN白色沉淀 | B、当Ag+定量沉淀后,少许过量的SCN-与Fe3+生成红色配合物,即为终点 | C、上述实验可用KCl标准溶液代替KSCN的标准溶液滴定Ag+ | D、滴定时,必须控制溶液一定的酸性,防止Fe3+水解,影响终点的观察 |