水是一种非常难电离的物质.250C时,水的离子积Kw=1.0×10-14.下列有关水的叙述正确的是( )
| A、水是一种非电解质 | B、纯水中c(H+)随着温度的升高而降低 | C、250C时,pH相同的NaOH溶液与醋酸钠溶液,水的电离度前者小于后者 | D、由液态水结成冰的过程是一个熵增的过程 |
纯水呈中性,这是因为( )
| A、纯水pH=7 | B、纯水中无H+也无OH- | C、纯水中c(H+)=c(OH-) | D、纯水的离子积KW=1.0×10-14 |
100℃,KW=1.0×10-12,若在此温度时,某溶液中的c(H+)=1.0×10-7mol/L,则该溶液( )
| A、呈中性 | B、呈碱性 | C、呈酸性 | D、1000c(H+)=c(OH-) |
下列操作中,能使水的电离平衡H2O?H++OH-向右移动且溶液呈酸性的是( )
| A、向水中加入KHSO4溶液 | B、向水中加入KAl(SO4)2溶液 | C、向水中加入Na2CO3溶液 | D、将水加热到100℃,使pH=6 |
水是人体细胞的重要组成成分.下列有关水的说法错误的是( )
| A、食物代谢不会产生水 | B、水可作为体内生化反应的介质 | C、水在体内是一种很好的溶剂 | D、水可调节体温 |
 水的电离平衡曲线如图所示,若以A点表示25℃时水的电离达平衡时的离子浓度,B点表示100℃时水的电离达平衡时的离子浓度,则下列说法正确的是( )
水的电离平衡曲线如图所示,若以A点表示25℃时水的电离达平衡时的离子浓度,B点表示100℃时水的电离达平衡时的离子浓度,则下列说法正确的是( )| A、纯水中25°C时的,c(H+)比100℃的时c(H+)大 | B、100℃时某溶液中由水电离产生的c(H+)═1×10-11mol?L-1,则该溶液的Ph可能是11或3 | C、将pH=9的Ba(OH)2溶液与pH=4的稀盐酸混合,并保持100℃的恒温,混合溶液的pH=7,则Ba(OH)2溶液和盐酸的体积比为10:1 | D、25℃时,某Na2SO4溶液中c(SO 42-)=5.0×10-4mol/L则溶液中c(Na+):c(OH-)为104:1 |
下列物质加入水中,对水的电离能产生促进作用的是( )
| A、NH4Cl | B、NaOH | C、NaCl | D、H2SO4 |
将纯水加热至80℃,下列叙述正确的是( )
| A、水的离子积不变 | B、水的pH减小,呈酸性 | C、水的pH增大,呈中性 | D、c(H+)=c(OH-) |
能使水的电离平衡向右移动,且所得溶液呈碱性的是( )
| A、在水中加入Na2CO3固体 | B、在水中加入AlCl3固体 | C、在水中通入HCl气体 | D、将水加热至80℃ |
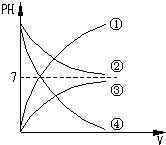 在如图①、②、③、④四条曲线中,能正确表示将一定浓度的NaOH溶液加水稀释,其pH与加水的体积(V)的关系的是( )
在如图①、②、③、④四条曲线中,能正确表示将一定浓度的NaOH溶液加水稀释,其pH与加水的体积(V)的关系的是( )