现有可逆反应:2A(g)+2B(g)?C(g)+3D(g),在密闭容器的容积、温度都相同的条件下,分别从以下两条途径建立平衡:
Ⅰ.A、B的起始物质的量均为2mol,
Ⅱ.C、D的起始物质的量分别为2mol和6mol.
以下说法中不正确的是( )
Ⅰ.A、B的起始物质的量均为2mol,
Ⅱ.C、D的起始物质的量分别为2mol和6mol.
以下说法中不正确的是( )
| A、Ⅰ、Ⅱ两条途径最终达到平衡时,体系内混合气体的百分组成相同 | B、Ⅰ、Ⅱ两条途径最终达到平衡时,体系内混合气体的平均相对分子质量相同 | C、达到平衡时,Ⅰ途径A的平衡浓度等于Ⅱ途径A的平衡浓度 | D、达到平衡时,Ⅰ途径所得混合气密度为Ⅱ途径所得混合气密度的2倍 |
已知2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ?mol-1.在相同温度和体积均为1L的四个密闭容器中,保持温度和容积不变,以四种不同的投料进行反应,平衡时有关数据如下.下列关系正确的是( )
| 容器 | 甲 | 乙 | 丙 | 丁 |
| 起始加入量 | 2mol SO2+1mol O2 | 1mol SO2+0.5mol O2 | 2mol SO3 | 2mol SO2+2mol O2 |
| 反应放出或吸收的热量/kJ | a | b | c | d |
| 平衡时c(SO3)/mol?L-1 | e | f | g | h |
| A、a<2b:e>2f |
| B、a=c:e=g |
| C、a>d:e>h |
| D、c+98.3e=196.6 |
在密闭容器中,加入3mol A和1mol B,一定条件下发生反应3A(g)+B(g)?2C(g)+D(g),达平衡时,测得C的浓度为w mol/L,若保持体积和温度不变,重新按下列配比作起始物质,达到平衡时,C的浓度仍然为w mol/L的是( )
| A、6mol A+2mol B | B、1.5mol A+0.5mol B+1mol C+0.5mol D | C、3mol A+1mol B+2mol C+1mol D | D、4mol C+1mol D |
向容积相同的甲、乙密闭容器中投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下(已知N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ?mol-1):
下列说法正确的是( )
| 反应物投入量 | NH3的浓度 (mol?L-1) |
反应的 能量变化 |
体系压强 (Pa) |
反应物 转化率 | |
| 甲 | 1mol N2、3mol H2 | c1 | 放出a kJ | p1 | α1 |
| 乙 | 2mol NH3 | c2 | 吸收b kJ | p2 | α2 |
| A、c1=c2 |
| B、a+b=1 |
| C、p1>p2 |
| D、α1+α2>1 |
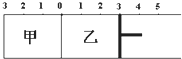 如图所示,甲容器容积固定不变,乙容器有可移动的活塞.甲中充入2mol SO2和1mol O2,乙中充入2mol SO3和1mol He,在恒定温度和催化剂条件下,甲、乙达到如下平衡:
如图所示,甲容器容积固定不变,乙容器有可移动的活塞.甲中充入2mol SO2和1mol O2,乙中充入2mol SO3和1mol He,在恒定温度和催化剂条件下,甲、乙达到如下平衡:2SO3(g)?2SO2(g)+O2(g).
根据活塞位置,下列有关说法正确的是( )
| A、若活塞固定在3处不动,达平衡时两容器中的压强相等 | B、若活塞固定在3处不动,达平衡时两容器中SO3的浓度相等 | C、若活塞固定在4处不动,达平衡时两容器中SO3的物质的量分数相等 | D、若活塞固定在5处不动,达平衡时乙容器中SO2的物质的量较小 |
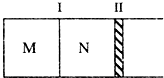 如图所示,隔板Ⅰ固定不动,活塞Ⅱ可自由移动.M、N两个容器中均发生如下反应:A(g)+3B(g)?2C(g);△H<0.若起始时,M、N容积相同.下列说法正确的是( )
如图所示,隔板Ⅰ固定不动,活塞Ⅱ可自由移动.M、N两个容器中均发生如下反应:A(g)+3B(g)?2C(g);△H<0.若起始时,M、N容积相同.下列说法正确的是( )| A、起始时,分别向M、N两个容器中加入1molA、1molC,达平衡时,容器M、N中物质A的体积分数相同 | B、起始时,分别向M、N两个容器中加入1molA、3molB,达平衡时,容器M中物质A的转化率较大 | C、起始时,分别向M、N两个容器中加入2molC,容器N达到平衡所需的时间较短 | D、起始时,分别向M、N两个容器中加入1molA、3molB,达平衡时,容器M中气体的密度较大 |
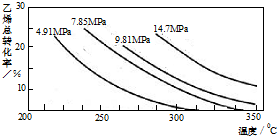 工业上采用乙烯和水蒸气在催化剂(磷酸/硅藻土)表面合成乙醇,反应原理为:CH2=CH2(g)+H2O(g)?CH3CH2OH(g),副产物有乙醛、乙醚及乙烯的聚合物等.下图是乙烯的总转化率随温度、压强的变化关系,下列说法正确的是( )
工业上采用乙烯和水蒸气在催化剂(磷酸/硅藻土)表面合成乙醇,反应原理为:CH2=CH2(g)+H2O(g)?CH3CH2OH(g),副产物有乙醛、乙醚及乙烯的聚合物等.下图是乙烯的总转化率随温度、压强的变化关系,下列说法正确的是( )| A、合成乙醇的反应一定为吸热反应 | B、目前工业上采用250~300℃,主要是在此温度下乙烯的转化率最大 | C、目前工业上采用加压条件(7MPa左右),目的是提高乙醇的产率和加快反应速率 | D、相同催化剂下,在300℃14.7MPa乙醇产率反而比300℃7MPa低得多,是因为加压平衡向逆反应方向移动 |
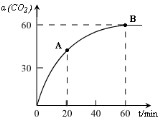 工业上合成尿素是用CO2和NH3在一定条件下合成,其反应方程式为2NH3+CO2
工业上合成尿素是用CO2和NH3在一定条件下合成,其反应方程式为2NH3+CO2| 一定条件 |
| n(NH3) |
| n(CO2) |
| A、该反应在60min时达到平衡状态 |
| B、NH3的平衡转化率为30% |
| C、增加氨碳比可进一步提高CO2的平衡转化率 |
| D、A点的逆反应速率υ逆(CO2)大于B点的正反应速率υ正(CO2) |
取五等份NO2,分别加入温度不同、容积相同的恒容密闭容器中,发生反应:2NO2(g)?N2O4(g)△H<0反应相同时间后,分别测定体系中NO2的百分量(NO2%),并作出其随反应温度(T)变化的关系图.下列示意图中,可能与实验结果相符的是( )
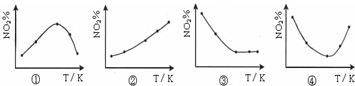

| A、②④ | B、② | C、①② | D、③④ |
某校化学研究性学习小组的同学研究了在其他条件不变时,只改变一个条件对以下可逆反应的影响:2SO2(g)+O2(g)?2SO3(g);△H<0,则下列有关说法正确的是( )
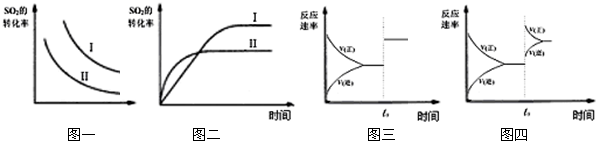

| A、图一研究的是温度、压强对平衡的影响,横坐标表示压强 | B、图二研究的是温度对平衡的影响,Ⅱ采用的温度更高 | C、图三中t0时使用了催化剂,使平衡向正反应方向进行 | D、图四中t0时增大了SO2的浓度,使平衡向正反应方向进行 |