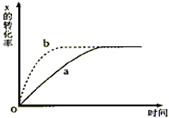
 如图曲线a表示放热反应X(g)+Y(g)?Z(g)+M(g)+N(s)进行过程中X的转化率随时间变化的关系.若要改变起始条件,使反应过程按b曲线进行,可采取的措施是( )
如图曲线a表示放热反应X(g)+Y(g)?Z(g)+M(g)+N(s)进行过程中X的转化率随时间变化的关系.若要改变起始条件,使反应过程按b曲线进行,可采取的措施是( )| A、升高温度 | B、加大X的投入量 | C、恒温恒容充入氖气 | D、恒温缩小容器体积 |
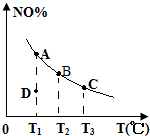 某密闭容器中存在2NO+O2?2NO2反应,平衡时NO的转化率与温度变化关系如图所示(曲线上任何一点都表示平衡状态),下列说法中正确的是( )
某密闭容器中存在2NO+O2?2NO2反应,平衡时NO的转化率与温度变化关系如图所示(曲线上任何一点都表示平衡状态),下列说法中正确的是( )| A、该反应的正反应是吸热反应 | B、若温度为T1、T3时的平衡常数分别为K1、K3,则K1<K3 | C、T1时,当反应处于D点,则该反应的逆反应速率大于正反应速率 | D、如果缩小容器体积,则平衡时表示NO转化率与温度变化关系的曲线在原曲线上方 |
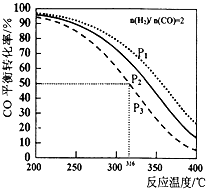 二甲醚是一种清洁燃料,以n(H2)/n(CO)=2通入1L的反应器中,一定条件下发生反应:2CO(g)+4H2(g)?CH3OCH3(g)+H2O(g)△H,其CO的平衡转化率随温度、压强变化关系如图所示,下列说法正确的是( )
二甲醚是一种清洁燃料,以n(H2)/n(CO)=2通入1L的反应器中,一定条件下发生反应:2CO(g)+4H2(g)?CH3OCH3(g)+H2O(g)△H,其CO的平衡转化率随温度、压强变化关系如图所示,下列说法正确的是( )| A、上述反应△H>0 | B、图中P1<P2<P3 | C、若在P3和316℃时,测得容器中n(H2)=n(CH3OCH3),此时v(正)<v(逆) | D、若在P3和316℃时,起始时n(H2)/n(CO)=3,则达到平衡时,CO转化率小于50% |
下列图示与对应的叙述相符的是( )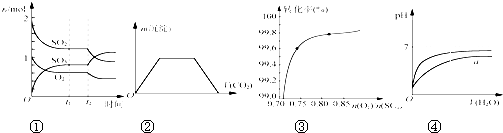

A、图①表示一定条件下进行的反应2SO2+O2
| |||
| B、图②表示向Ba(OH)2、KAlO2混合溶液中通入CO2 | |||
C、如图③在其他条件不变时,2SO2(g)+O2(g)
| |||
| D、图④表示pH相同的盐酸与醋酸中分别加入水后pH的变化,其中曲线a对应的是盐酸 |
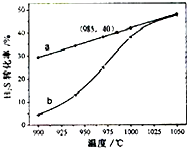 H2S受热分解的反应为:2H2S(g)→2H2(g)+S2(g).在恒温密闭容器中,控制不同温度进行 H2S分解实验.以H2S起始浓度均为cmol?L-1测定H2S的转化率,结果如图.图中a曲线为H2S 的平衡转化率与温度关系,b曲线表示不同温度下反应经过相同时间的转化率.下列叙述错误的是( )
H2S受热分解的反应为:2H2S(g)→2H2(g)+S2(g).在恒温密闭容器中,控制不同温度进行 H2S分解实验.以H2S起始浓度均为cmol?L-1测定H2S的转化率,结果如图.图中a曲线为H2S 的平衡转化率与温度关系,b曲线表示不同温度下反应经过相同时间的转化率.下列叙述错误的是( )A、985℃时,H2S按上述反应分解的平衡常数K=
| ||
| B、H2S的分解为吸热反应 | ||
| C、图象能解释,温度升高,反应速率加快 | ||
| D、如果只将上述条件中的温度改为压强,图象的形式基本不变 |
甲醇脱氢可制取甲醛CH3OH(g)?HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如图所示.下列有关说法正确的是( )
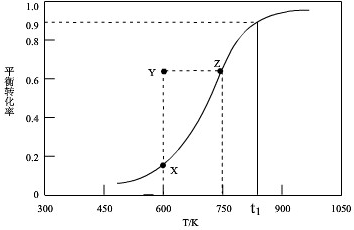

| A、脱氢反应的△H<0 | B、600K时,Y点甲醇的υ(正)<υ(逆) | C、从Y点到Z点可通过增大压强 | D、在t1K时,该反应的平衡常数为8.1mol?L-1 |
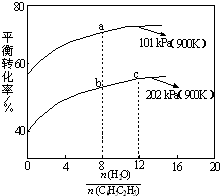 苯乙烯(C6H5CH=CH2)是生产各种塑料的重要单体,其制备原理是:C6H5C2H5(g)?C6H5CH=CH2(g)+H2(g),实际生产中常以高温水蒸气作为反应体系的稀释剂(水蒸气不参加反应),如图为乙苯的平衡转化率与水蒸气的用量、体系总压强的关系.下列说法正确的是( )
苯乙烯(C6H5CH=CH2)是生产各种塑料的重要单体,其制备原理是:C6H5C2H5(g)?C6H5CH=CH2(g)+H2(g),实际生产中常以高温水蒸气作为反应体系的稀释剂(水蒸气不参加反应),如图为乙苯的平衡转化率与水蒸气的用量、体系总压强的关系.下列说法正确的是( )| A、a点转化率为75%,若起始向1 L恒容容器中充入1 mol 乙苯,则平衡常数为2.25 | ||
B、b点转化率为50%,则混合气体中苯乙烯的体积分数为
| ||
| C、恒容时加入稀释剂能减小C6H5C2H5平衡转化率 | ||
| D、b点和c点温度和压强相同,所以反应速率也相等 |
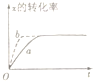 如图所示,曲线a表示放热反应x(g)+Y(g)?z+M(g)进行过程中x的转化率随时间变化的关系.若要改变起始条件,使反应按曲线b进行,可采取的措施是( )
如图所示,曲线a表示放热反应x(g)+Y(g)?z+M(g)进行过程中x的转化率随时间变化的关系.若要改变起始条件,使反应按曲线b进行,可采取的措施是( )| A、升高温度 | B、加大x的投入量 | C、增大体积 | D、加催化剂 |
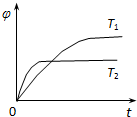 一定条件下,将一定量的A、B、C、D四种物质,置于密闭容器中发生如下反应:
一定条件下,将一定量的A、B、C、D四种物质,置于密闭容器中发生如下反应:m A(s)+n B(g)═p C(g)+q D(g)△H 达到平衡后,测得B的浓度为0.5mol/L.保持温度不变,将密闭容器的容积扩大到原来的两倍,再次达到平衡后,测得B的浓度为0.3mol?L-1.当其它条件不变时,C在反应混合物中的体积分数(φ)与温度(T)、时间(t)的关系如图所示.下列叙述正确的是( )
| A、热化学方程式中:n<p+q | B、热化学方程式中:△H>0 | C、达平衡后,增加A的量,有利于提高B的转化率 | D、若T1、T2时反应的平衡常数分别为K1、K2,则K1>K2 |
下列图示与对应的叙述相符的是( )
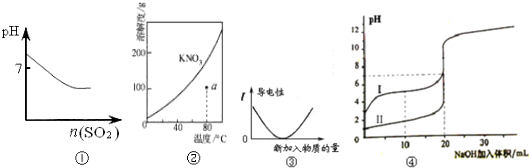

| A、图①可表示将SO2气体通入溴水时pH的变化 | B、图②表示KNO3的溶解度曲线,a点是80℃的KNO3的不饱和溶液 | C、图③表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化 | D、图④表示室温下,0.100mol/L NaOH溶液分别滴定0.100mol/L的盐酸和醋酸的滴定曲线,由图知Ⅰ为盐酸的滴定曲线 |