 容积均为1L的甲、乙两个恒容容器中,分别充入2mol A、2mol B和1mol A、1mol B,相同条件下,发生下列反应:A(g)+B(g)?xC(g)△H<0.测得两容器中c(A)随时间t的变化如图所示,下列说法正确的是( )
容积均为1L的甲、乙两个恒容容器中,分别充入2mol A、2mol B和1mol A、1mol B,相同条件下,发生下列反应:A(g)+B(g)?xC(g)△H<0.测得两容器中c(A)随时间t的变化如图所示,下列说法正确的是( )| A、该反应的x=3 | B、此条件下,该反应的平衡常数K=4 | C、给乙容器升温可缩短反应达平衡的时间也能提高平衡转化率 | D、其他条件不变,向甲容器中再充入0.2mol C,平衡时A的体积分数增大 |
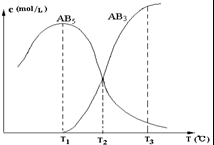 在一密闭的容器中,由一定量的A4(s)和B2(g)反应,可得到AB5(g)和AB3(g)二种产物,生成物在各个温度下的平衡浓度c与温度T的关系如图.下列说法错误的是( )
在一密闭的容器中,由一定量的A4(s)和B2(g)反应,可得到AB5(g)和AB3(g)二种产物,生成物在各个温度下的平衡浓度c与温度T的关系如图.下列说法错误的是( )| A、AB5(g)?AB3(g)+B2(g)其反应的反应热△H>0 | B、A4(s)+10B2(g)?4AB5(g)其反应的反应热△H<0 | C、在T2时刻,保持温度不变,给体系加压,达到新平衡时,n(AB5)>n(AB3) | D、在T1、T2、T3时,容器中B2的物质的量的大小关系为n(B2,T3)>n(B2,T2)>n(B2,T1) |
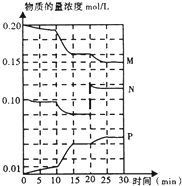 如图所示是某反应体系中的三种气态物质M、N、P的物质的量浓度随时间的变化情况,则下列判断不正确的是( )
如图所示是某反应体系中的三种气态物质M、N、P的物质的量浓度随时间的变化情况,则下列判断不正确的是( )| A、该反应的化学方程式可表达为2M+N?2P | B、当反应时间为20 min时,曲线开始发生变化的原因可能是由于增大压强引起的 | C、反应在10 min时,若曲线的变化是由于升温造成的(其他条件不变),则该反应的正反应一定为吸热反应 | D、在反应时间段10 min~15 min内,物质P的反应速率约为0.0001 mol/(L?s) |
 把1 mol CO2和3mol H2通入1 L的密闭容器中,在某温度下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ?mol-1
把1 mol CO2和3mol H2通入1 L的密闭容器中,在某温度下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ?mol-1测得CO2和CH3OH的浓度随时间变化如图所示,下列说法正确的是( )
| A、3min时,v正=v逆 | B、0~10 min内,氢气的平均反应速率为0.225 mol?L-1?min-1 | C、该温度下,反应的平衡常数K=5.3 mol-2?L2 | D、若升高温度,CO2的平衡转化率大于75% |
向两个容积均为1L的恒容容器甲、乙中,分别充入2molA、2molB和1molA、1molB,在相同温度下发生反应:A(g)+B(g)?xC(g);△H<0.测得两容器中c(A)随时间t的变化如图所示.下列说法正确的是( )
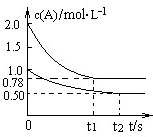

| A、x≤2 | B、甲容器中用B的浓度变化表示的该反应在t1秒内的平均反应速率为0.78/t1mol/(L?s) | C、其它条件不变,降低乙容器的温度,乙中A的平衡转化率将大于50% | D、其它条件不变,向平衡后的甲容器中再充入2molA、2molB,则达新平衡时甲中A的浓度为1.56mol/L |
已知C0和H2在一定条件下合成甲醇的反应为:CO(g)+2M2(g)?CH30H(g)现在容积均为1L的a、b、c三个密闭容器中分别充入1mol C0和2mol H2的混合气体,控制温度,进行反应,测得相关数据的关系如图1和图2所示.下列说法正确的是( )


| A、该反应的正反应的△H<0 | B、反应进行到5min时,a容器中v(正)=v(逆) | C、升温或减压,可将b中的平衡状态转变成c中的平衡状态 | D、达到平衡时,a、b、c中C0的转化率为b>a>c |
如图表示反应X(g)+4Y(g)?5Z△H<0(g),在某温度时X的浓度随时间变化的曲线下列有关该反应的描述正确的是.( )
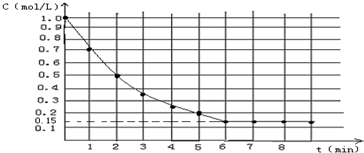

| A、若Z是有色气体,只压缩容器的体积,平衡不移动,则气体颜色不变 | B、若升高温度,则X的平衡转化率减小,υ(逆)增大,υ(正)减小 | C、若X和Y的平衡转化率相等,则起始时X和Y的物质的量之比为1:4 | D、若平衡时X的转化率为85%,则起始时Y的物质的量浓度为3.4mol?L-1 |
 将CO2转化成甲醇燃料是减排,环保的一种科学方法,其原理
将CO2转化成甲醇燃料是减排,环保的一种科学方法,其原理为:CO2(g)+3H2(g)
| 一定条件 |
△H<0500℃时,在体积为lL的固定容积密闭容器中充人
lmol CO2,3mol H2,测得CO2浓度与甲醇浓度随时间变
化如图所示;从中得出下列结论中错误的( )
| A、曲线x表示可以CH3OH浓度变化,曲线Y表示CO2浓度变化 |
| B、从反应开始到平衡,氢气的反应速率v(H2)=0.225mol/(L?min) |
| C、平衡时H2的转化率为75% |
| D、该反应的平衡常数K=3 |
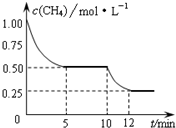 在密闭容器中进行反应CH4(g)+H2O(g)?CO(g)+3H2(g)△H>0,测得c(CH4)随反应时间(t)的变化如图所示.下列判断正确的是( )
在密闭容器中进行反应CH4(g)+H2O(g)?CO(g)+3H2(g)△H>0,测得c(CH4)随反应时间(t)的变化如图所示.下列判断正确的是( )| A、0~5 min内,v(H2)=0.1 mol?(L?min)-1 | B、反应进行到12min时,CH4的转化率为25% | C、恒温下,缩小容器体积,平衡后H2浓度减小 | D、10 min时,改变的外界条件可能是升高温度 |
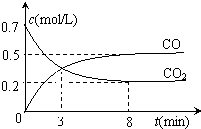 一定条件下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,发生反应:Fe(s)+CO2(g)?FeO(s)+CO(g)△H>0.反应过程中CO2气体和CO气体的浓度与时间的关系如图所示,下列说法不正确的是( )
一定条件下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,发生反应:Fe(s)+CO2(g)?FeO(s)+CO(g)△H>0.反应过程中CO2气体和CO气体的浓度与时间的关系如图所示,下列说法不正确的是( )A、该反应的平衡常数表达式为K=
| ||
B、升高温度后达新平衡时,
| ||
| C、3分钟时,CO和CO2的浓度相等,反应达到平衡状态 | ||
| D、8分钟内CO的平均反应速率v(CO)=0.0625 mol?L-1?min-1 |