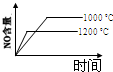
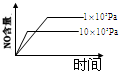
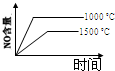
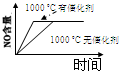
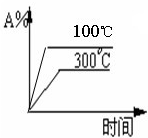
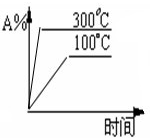
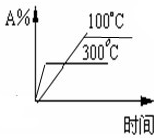
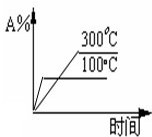
在体积一定的密闭容器中,给定物质A、B、C的量,在一定条件下发生反应,建立如下化学平衡:aA(g)+bB(g)?xC(g),符合图1所示的关系(c%表示平衡混合气中产物C的百分含量,T表示温度,p表示压强).在图2中,Y轴是指( )
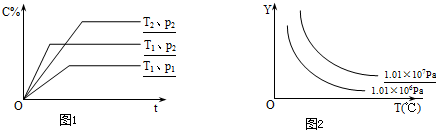
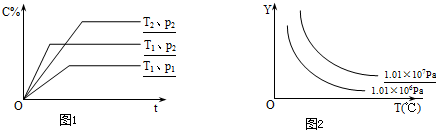
| A、反应物A的百分含量 | B、反应物B的平衡转化率 | C、平衡混合气的密度 | D、平衡混合气的总物质的量 |
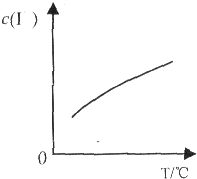 已知:I2与KI溶液发生如下反应:I2(aq)+I-(aq)?I3-(aq),达到平衡后溶液中I-的平衡浓度c(I-)随温度T的变化如图所示.下列有关说法正确的是
已知:I2与KI溶液发生如下反应:I2(aq)+I-(aq)?I3-(aq),达到平衡后溶液中I-的平衡浓度c(I-)随温度T的变化如图所示.下列有关说法正确的是( )
| A、固体碘微溶于水,实验室配制较浓“碘水”时,可将固体碘溶于一定浓度的KI溶液中 | B、反应I2(aq)+I-(aq)?I3-(aq)的△H>0 | C、在I2的KI水溶液中加入CCl4或H2O2均可使溶液中c(I3-)增大 | D、依此原理,Cl2在一定浓度的NaCl溶液中溶解度增大 |
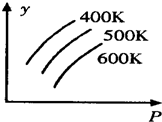 如图中表示外界条件(T、P)的变化对下列反应的影响L(固)+G(气)?2R(气);△H>0,y轴表示的是( )
如图中表示外界条件(T、P)的变化对下列反应的影响L(固)+G(气)?2R(气);△H>0,y轴表示的是( )| A、平衡时,混合气中R的百分含量 | B、平衡时,混合气中G的百分含量 | C、G的转化率 | D、L的转化率 |
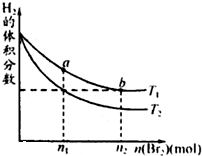 在体积为VL的恒容密闭容器中盛有一定量H2,通入Br2(g)发生反应:H2(g)+Br2(g)?2HBr(g);△H<0. 当温度分别为T1、T2达平衡时,H2的体积分数与Br2(g)的物质的量变化关系如图所示.下列说法不正确的是( )
在体积为VL的恒容密闭容器中盛有一定量H2,通入Br2(g)发生反应:H2(g)+Br2(g)?2HBr(g);△H<0. 当温度分别为T1、T2达平衡时,H2的体积分数与Br2(g)的物质的量变化关系如图所示.下列说法不正确的是( )| A、由图可知:T1>T2 | B、a、b两点的反应速率:b>a | C、为了提高Br2(g)的转化率,可采取将HBr液化并及时移走的方法 | D、T1时,随着Br2(g)加入,平衡时HBr的体积分数不断增加 |
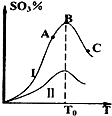 硫酸生产中炉气转化反应为:2SO2(g)+O2(g)?2SO3(g).研究发现,SO3的体积分数(SO3%)随温度(T)的变化如曲线I所示.下列判断正确的是( )
硫酸生产中炉气转化反应为:2SO2(g)+O2(g)?2SO3(g).研究发现,SO3的体积分数(SO3%)随温度(T)的变化如曲线I所示.下列判断正确的是( )| A、该反应的正反应为吸热反应 | B、反应达到B点时,2v正(O2)=v逆(SO3) | C、曲线I上A、C两点反应速率的关系是:vA>vC | D、已知V2O5的催化效果比Fe2O3好,若I表示用V2O5催化剂的曲线,则II是Fe2O3作催化剂的曲线 |
在某一密闭容器中,充入一定量的HI气体,发生反应2HI(g)?H2(g)+I2(g);△H>0,在t1时达到平衡,t2时加热升温并保温,到t3时又达到新平衡,符合这一变化的图象是( )
A、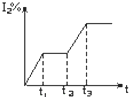 | B、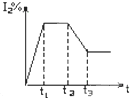 | C、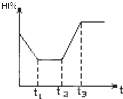 | D、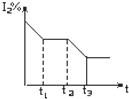 |
常用图象直观地描述化学反应的进程或结果.下列有关图象的描述正确的是( )


| A、图①可表示温度对“A2(g)+3B2(g)?2AB3(g)△H<0”的影响 | B、图①可表示压强对2A(g)+2B(g)?3C(g)+D(s)的影响 | C、图②可表示醋酸溶液中通入氨气至过量,溶液导电性的变化 | D、图②可表示Ba(OH)2溶液中滴加稀硫酸,溶液导电性的变化 |
反应A(?)+aB(g)?C(g)+2D(g)(a为正整数).反应过程中,当其他条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图所示.下列说法不正确的是( )


| A、若a=2,则A为液态或固体 | B、该反应的正反应为放热反应 | C、T2>T1,P2>P1 | D、其他条件不变,增加B的物质的量,平衡正向移动,平衡常数K增大 |