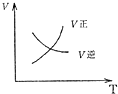
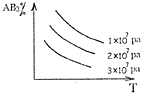
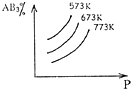
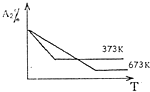
在某容积一定的密闭容器中,可逆反应:A(g)+B(g)?xC(g),符合如图(I)所示关系,由此推断关于图(Ⅱ)的说法正确的是( )
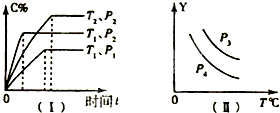
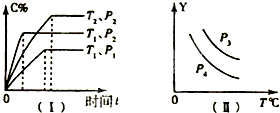
| A、若P3<P4,y轴表示B的百分含量 | B、若P3>P4,y轴表示A的转化率 | C、若P3>P4,y轴表示混合气体的密度 | D、若P3<P4,y轴表示混合气体的平均相对分子质量 |
向甲、乙两个容积均为1L的恒容容器中,分别充入2mol A、2mol B和1mol A、1mol B.相同温度下,发生反应:A(g)+B(g)?xC(g);△H<0.测得两容器中c(A)随时间t的变化如图所示.下列说法正确的是( )
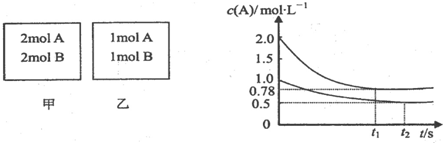

| A、x不可能等于2 | B、甲、乙两容器中反应达平衡时,平衡常数K(甲)<K(乙) | C、将乙容器升温可使甲、乙容器内各物质的体积分数相同 | D、若向甲容器中再充入2 mol A、2 mol B,则平衡时甲容器中0.78 mol?L-1<c(A)<1.56 mol?L-1 |
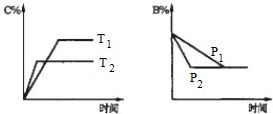 可逆反应aA(s)+bB(g)?cC(g)+dD(g)△H=Q,反应过程中,当其他条件不变时,某物质在混合物中的含量与温度(T)、压强(p)的关系如图所示据图分析,以下正确的是( )
可逆反应aA(s)+bB(g)?cC(g)+dD(g)△H=Q,反应过程中,当其他条件不变时,某物质在混合物中的含量与温度(T)、压强(p)的关系如图所示据图分析,以下正确的是( )| A、T1>T2,Q>0 | B、Tl<T2,Q>0 | C、P1>P2,a+b=c+d | D、Pl<P2,b=c+d |
如图反应中,同时符合图象Ⅰ和Ⅱ的是( )
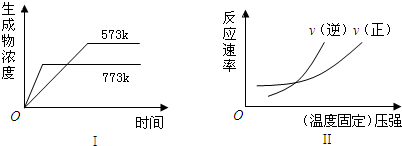

| A、N2(g)+3H2(g)?2NH3(g)△H<0 | B、2SO3(g)?2SO2(g)+O2(g)△H>0 | C、H2(g)+CO(g)?C(s)+H2O(g)△H>0 | D、4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H<0 |
下列图示与对应的叙述相符的是( )
A、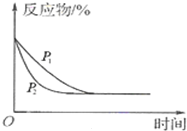 图表示压强对反应2A(g)+2B(g)═3C(g)+D(s)的影响,且P2>PI | B、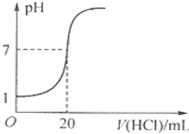 如图表示25℃时,用0.1 mol/L盐酸滴定20mL 0.1mol/L NaOH溶液,溶液的pH随加入盐酸体积的变化 | C、 依据如图,若除去CuSO4溶液中的Fe3+,可向溶液中加入适量CuO,调节pH≈4 | D、 图中开关K置于A或B处均可以减缓铁的腐蚀 |
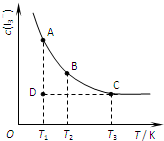 实验室中配制碘水,往往是将I2溶于KI溶液中,即可得到浓度较大的碘水,原因是发生了反应:I2(aq)+I-(aq)?I3-(aq).在反应的平衡体系中,c(I3-)与温度T的关系如图所示(曲线上的任何一点都表示平衡状态).下列说法正确的是( )
实验室中配制碘水,往往是将I2溶于KI溶液中,即可得到浓度较大的碘水,原因是发生了反应:I2(aq)+I-(aq)?I3-(aq).在反应的平衡体系中,c(I3-)与温度T的关系如图所示(曲线上的任何一点都表示平衡状态).下列说法正确的是( )| A、该反应的正反应为放热反应 | B、A状态与C状态的化学反应速率大小为v(A)>v(C) | C、D状态时,v正>v逆 | D、欲配制浓度较大的氯水,可将氯气通入氯化钾溶液中 |
 向2L的密闭容器中充入7.6mol NO和3.8mol O2,发生如下反应:
向2L的密闭容器中充入7.6mol NO和3.8mol O2,发生如下反应:①2NO(g)+O2 (g)?2NO2(g)
②2NO2(g)?N2O4(g)
测得NO2和N2O4的浓度变化如图所示,0~10min维持容器温度为T1℃,10min后升高并维持容器的温度为T2℃.下列说法正确的是( )
| A、前5min反应的平均速率v(N2O4)=0.18mol?(L?min)-1 | B、T1℃时反应②的化学平衡常数K=0.6 | C、反应①、②均为吸热反应 | D、若起始时向该容器中充入3.6mol NO2和2.0mol N2O4,T1℃达到平衡时,N2O4的转化率为10% |
下列图示与对应的叙述相符的是( )
A、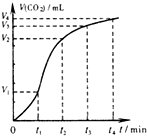 表示碳酸钙与盐酸反应收集到气体最多的时间段是t3~t4 | B、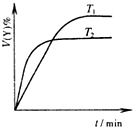 表示可逆反应“2X(g)?Y(g)△H<0”温度T1<T2的情形 | C、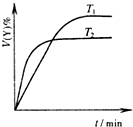 表示可逆反应“2X(g)?Y(g)△H<0”温度T1>T2的情形 | D、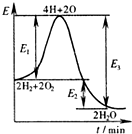 表示各物质发生反应的能量变化关系有E1=E2+E3 |
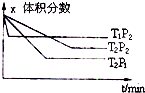 反应aX(g)+bY(g)?cZ(g);△H=Q,有如图所示关系,下列判断中正确是( )
反应aX(g)+bY(g)?cZ(g);△H=Q,有如图所示关系,下列判断中正确是( )| A、a+b<c,Q>0 | B、a+b<c,Q<0 | C、a+b>c,Q>0 | D、a+b>c,Q<0 |