已知:
(1)2Fe(s)+O2(g)=2FeO(s)△H=-544kJ?mol-1
(2)2Al(s)+
O2(g)=Al2O3(s)△H=-1675kJ?mol-1
则 2Al(s)+3FeO(s)=Al2O3(s)+3Fe(s)的△H为( )
(1)2Fe(s)+O2(g)=2FeO(s)△H=-544kJ?mol-1
(2)2Al(s)+
| 3 |
| 2 |
则 2Al(s)+3FeO(s)=Al2O3(s)+3Fe(s)的△H为( )
| A、-2491 kJ?mol-1 |
| B、+859 kJ?mol-1 |
| C、-1403 kJ?mol-1 |
| D、-859 kJ?mol-1 |
已知胆矾溶于水时溶液温度降低.胆矾分解的热化学方程式为CuSO4?5H2O(s)
CuSO4(s)+5H2O(l)△H=+Q1 mol?L-1.室温下,若将1mol无水硫酸铜溶解为溶液时放热Q2 kJ,则Q1与Q2的关系为( )
| ||
| A、Q1>Q2 |
| B、Q1=Q2 |
| C、Q1<Q2 |
| D、无法比较 |
已知下列数据:
2Fe(s)+O2(g)=2FeO(s)△H=-544kJ?mol-1
4Al(s)+3O2(g)=2Al2O3(s)△H=-3350kJ?mol-1
则2Al(s)+3FeO(s)=Al2O3(s)+3Fe(s)的△H是( )
2Fe(s)+O2(g)=2FeO(s)△H=-544kJ?mol-1
4Al(s)+3O2(g)=2Al2O3(s)△H=-3350kJ?mol-1
则2Al(s)+3FeO(s)=Al2O3(s)+3Fe(s)的△H是( )
| A、-859 kJ?mol-1 | B、+859 kJ?mol-1 | C、-1403 kJ?mol-1 | D、-2491 kJ?mol-1 |
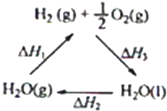
根据盖斯定律判断如图所示的物质转变过程中正确的是( )


| A、△H1=△H2=△H3=△H4 | B、△H1+△H2=△H3+△H4 | C、△H1+△H2+△H3=△H4 | D、△H1=△H2+△H3+△H4 |
 某科学家利用二氧化铈(CeO2)在太阳能作用下将H2O、CO2转变成H2、CO.其过程如下:
某科学家利用二氧化铈(CeO2)在太阳能作用下将H2O、CO2转变成H2、CO.其过程如下:mCeO2
| 太阳能 |
| ① |
(m-x)CeO2?xCe+xH2O+xCO2
| 900℃ |
| ① |
下列说法不正确的是( )
| A、该过程中CeO2没有消耗 |
| B、该过程实现了太阳能向化学能的转化 |
| C、图中△H1=△H2+△H3 |
| D、以CO和O2构成的碱性燃料电池的负极反应式为CO+4OH--2e-=CO32-+2H2O |
已知反应:①101kPa时,2C(s)+O2(g)═2CO(g)△H=-221kJ/mol
②稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ/mol
③H2(g)+
O2(g)═H2O(g)△H=-241.8kJ/mol
④H2O(g)═H2O(l)△H=-44.0kJ/mol
下列结论正确的是( )
②稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ/mol
③H2(g)+
| 1 |
| 2 |
④H2O(g)═H2O(l)△H=-44.0kJ/mol
下列结论正确的是( )
| A、碳的燃烧热大于110.5kJ/mol |
| B、浓硫酸与稀NaOH溶液反应生成1mol水,放出57.3kJ热量 |
| C、氢气的燃烧热为241.8 kJ/mol |
| D、2H2(g)+O2(g)═2H2O(l)的反应热为△H=-571.6 kJ/mol |
已知反应:①2C(s)+O2(g)=2CO(g)△H1=-221kJ/mol
②CO(g)+
O2(g)=CO2(g)△H2=-283kJ/mol
③稀溶液中,H+(aq)+OH-(aq)=H2O(l)△H3=-57.3kJ/mol
下列结论正确的是( )
②CO(g)+
| 1 |
| 2 |
③稀溶液中,H+(aq)+OH-(aq)=H2O(l)△H3=-57.3kJ/mol
下列结论正确的是( )
| A、12g C燃烧生成CO时,放出221kJ热量 | ||
| B、碳的燃烧热△H=-393.5kJ/mol | ||
C、CO(g)+
| ||
| D、稀醋酸与稀NaOH溶液反应生成1mol水时,放出57.3kJ热量 |
己知:HF(aq)与NaOH(aq)反应的△H=-67.7KJ?mol-1;HCl(aq)与NaOH(aq)反应的△H=-57.3KJ?mol-1.则HF在水溶液中电离的△H等于( )
| A、-10.4KJ?mol-1 | B、-125KJ?mol-1 | C、+10.4KJ?mol-1 | D、+125KJ?mol-1 |
白磷(P4)可由Ca3(PO4)2、焦炭和SiO2在一定条件下反应获得.相关热化学方程式如下:
2Ca3(PO4)2(s)+10C(s)═6CaO(s)+P4(s)+10CO(g)△H1=+3359.26kJ?mol-1
CaO(s)+SiO2(s)═CaSiO3(s)△H2=-89.61kJ?mol-1
2Ca3(PO4)2(s)+6SiO2(s)+10C(s)═6CaSiO3(s)+P4(s)+10CO(g)△H3
则△H3等于( )
2Ca3(PO4)2(s)+10C(s)═6CaO(s)+P4(s)+10CO(g)△H1=+3359.26kJ?mol-1
CaO(s)+SiO2(s)═CaSiO3(s)△H2=-89.61kJ?mol-1
2Ca3(PO4)2(s)+6SiO2(s)+10C(s)═6CaSiO3(s)+P4(s)+10CO(g)△H3
则△H3等于( )
| A、+3269.65kJ?mol-1 | B、+2821.6 kJ?mol-1 | C、+2821.6 kJ | D、+3896.92 kJ?mol-1 |
已知:H2(g)+
O2(g)═H2O(g)△H1=-241.8kJ?mol-1,C(s)+
O2(g)═CO(g)△H2=-110.5kJ?mol-1.由此可知焦炭与水蒸气反应的热化学方程式为:C(s)+H2O(g)═CO(g)+H2(g)△H3,则△H3为( )
| 1 |
| 2 |
| 1 |
| 2 |
| A、+131.3 kJ?mol-1 |
| B、-131.3 kJ?mol-1 |
| C、+352.3 kJ?mol-1 |
| D、-352.3 kJ?mol-1 |