A的化学式为NH5,常温下呈固态,构成它的所有原子的最外层都符合相应稀有气体原子的最外电子层结构.则下列有关说法中,不正确的是( )
| A、1mol NH5中含有5NA个N-H键(NA为阿佛加德罗常数的数值) | B、NH5中既有共价键,又有离子键 | C、它与水反应的化学方程式为:NH5+H2O═NH3?H2O+H2↑ | D、NH5的电子式为: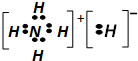 |
下列化学式能真实表示物质分子组成的是( )
| A、KOH | B、CO2 | C、SiO2 | D、Fe |
下列有关叙述中,错误的是( )
| A、金刚石的网状结构中,由共价键形成的最小碳环上有6个碳原子 | B、白磷分子晶体中,微粒之间通过共价键结合 | C、σ键可以单独存在,π键不可单独存在 | D、H2O的分解温度及沸点都比H2S高得多的事实不可都用氢键知识解释 |
若不断地升高温度,实现“雪花→水→水蒸气→氧气和氢气”的变化.在变化的各阶段被破坏的粒子间的主要相互作用依次是( )
| A、氢键 分子间作用力 非极性键 | B、氢键 氢键 极性键 | C、氢键 极性键 分子间作用力 | D、分子间作用力 氢键 非极性键 |
共价键、离子键和范德华力都是微观粒子之间的不同作用力,下列物质:①Na2O2、②SiO2、③NH4Cl、④金刚石、⑤CaH2、⑥白磷,其中含有两种结合力的组合是( )
| A、①③⑤⑥ | B、②④⑥ | C、①③⑥ | D、①②③⑥ |
下列各组物质熔化或升华时,所克服的粒子间作用力属于同种类型的是( )
| A、Na2O 和 SiO2 | B、冰和金刚石熔化 | C、氯化钠和蔗糖熔化 | D、碘和干冰升华 |
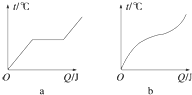 1、如图是a、b两种不同物质的熔化曲线,下列说法中正确的是( )
1、如图是a、b两种不同物质的熔化曲线,下列说法中正确的是( )①a是晶体 ②a是非晶体 ③b是晶体 ④b是非晶体.
| A、①④ | B、②④ | C、①③ | D、②③ |
下列说法中,不正确的是( )
| A、干冰升华,克服的是CO2的分子间作用力 | B、碳原子间连接方式的多样性,是含碳化合物种类繁多的原因之一 | C、航空航天等技术所需要的许多高新材料有赖于化学合成 | D、目前,科学家还无法实现对原子或分子的操纵 |
 以色列化学家丹尼尔?谢赫经因为发现准晶体而获得2011年诺贝尔化孚奖.准晶体原子里排列有序,但不具备普通晶体的长程平移对称性,而且原子位置之间有间隙(如图).下列说法不正确的是( )
以色列化学家丹尼尔?谢赫经因为发现准晶体而获得2011年诺贝尔化孚奖.准晶体原子里排列有序,但不具备普通晶体的长程平移对称性,而且原子位置之间有间隙(如图).下列说法不正确的是( )| A、石墨是原子晶体,0.12g石墨中约含6.02×1021个碳原子 | B、与类似普通晶体比较,准晶体延展性较低 | C、与类似将通晶体比较,准晶体密度较小 | D、普通玻璃属于非晶体,其成份中存在共价键 |
下列说法和推论均正确的是( )
| A、SiH4的沸点高于CH4,可推测PH3的沸点高于NH3 | B、NaCl晶体是离子晶体,可推测KCl晶体也是离子晶体,KCl晶体的熔点比NaCl晶体高 | C、NH4+为正四面体结构,可推测PH4+ 也为正四面体结构 | D、NaHCO3溶液呈碱性,可推测NaHSO3溶液、NaHS溶液也呈碱性 |