下列说法中,正确的是( )
| A、Na2O2 既含有离子键又含有非极性键 | B、化学键断裂时,会释放出能量 | C、离子化合物中阴阳离子间只存在静电引力 | D、HI比HCl易分解,说明H-I键比H-Cl键断裂耗能多 |
下列物质中属于含有极性键的分子晶体是( )
| A、金刚石 | B、食盐 | C、硫磺 | D、干冰 |
下列有关说法中不正确的是( )
| A、水电解过程中所吸收的能量主要用于克服分子间的作用力 | B、硫酸氢钠溶于水的过程中既有离子键被破坏又有共价键被破坏 | C、二氧化碳分子的结构式:O=C=O | D、乙酸分子的比例模型为: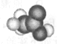 |
下列叙述中,结论(事实)和对应的解释(事实)均不正确的是( )
| A、金刚石的熔沸点高于晶体硅,因为C-C键能大于Si-Si键能 | B、二氧化硅晶体中不存在SiO2分子,因为它含有硅氧四面体的空间网状结构 | C、稀有气体的晶体属于原子晶体,因为其组成微粒是原子,不存在分子间作用力 | D、空间构型为正四面体结构的分子中,化学键的键角不一定是109°28′,有可能为60° |
下列有关叙述正确的是( )
| A、稀有气体的晶体其组成微粒是原子,晶体中不存在分子间作用力 | ||
| B、金刚石的熔沸点高于晶体硅,因为C-C键能大于Si-Si键能 | ||
C、CO燃烧的热化学方程式可表示为:CO(g)+
| ||
D、C-12的原子组成符号为
|
下列晶体在熔化时克服的作用力完全相同的是( )
| A、冰与干冰 | B、铝与氧化铝 | C、氯化钠与冰醋酸 | D、金刚石与二氧化硅 |
下列叙述及对应说明不正确的是( )
| A、金刚石的熔沸点高于晶体硅,因为 C-C 键比 Si-Si键强 | B、稀有气体的晶体属于原子晶体,因为其构成微粒是原子 | C、静电除尘治理悬浮颗粒污染,其依据是胶体的电泳原理 | D、丝织品不能用加酶洗衣粉洗涤,因为蛋白质在酶的作用下易水解 |
下列物质中熔点最高的是( )
| A、干冰 | B、氯化钠 | C、金刚石 | D、汞 |
下列说法正确的是( )
| A、氯化钠固体溶于水时离子键受到了破坏 | B、氨水能导电,氨气是点解质 | C、沸点:HF<HCI<HBr<HI | D、水分子中各原子均达到了8电子稳定结构 |
第ⅠA族元素的原子与第ⅦA族元素的原子结合形成的晶体属于( )
| A、离子晶体 | B、分子晶体 | C、原子晶体 | D、何种晶体无法确定 |