下列针对H3O+的说法中正确的是( )
| A、中心原子上的孤电子对数为2 | B、O原子采用sp2杂化,空间构型为三角锥形 | C、离子中存在配位键 | D、纯水呈中性,纯水中不存在H3O+微粒 |
关于SO2和CO2的说法中,正确的是( )
| A、都是V形分子 | B、中心原子上的孤电子对数相同 | C、都是极性分子 | D、它们形成的晶体类型相同 |
氰气分子式为(CN)2,结构式为NC-CN,和卤素单质分子具有相似的性质,下列叙述正确的是( )
| A、分子中含有3个σ键2个π键 | B、分子中CN的键长小于C-C键的键长 | C、(CN)2一定不和氢氧化钠溶液反应 | D、分子构型不可能是直线型 |
下列叙述错误的是( )
A、
| ||||
B、CO2的分子模型: | ||||
| C、在CS2、PCl3中各原子最外层均能达到8电子的稳定结构 | ||||
| D、熵增加且放热的反应一定是自发反应 |
CaC2是制取乙炔气体的原料,其中C22-与O22+互为等电子体,O22+的电子式可表示为 ;1mol O22+中含有的π键数目为 .
(3)X、Y两种有机物的分子结构和部分物理性质如下表,二者物理性质有差异的主要原因是 .
(3)X、Y两种有机物的分子结构和部分物理性质如下表,二者物理性质有差异的主要原因是
| 代号 | 结构简式 | 水中溶解度/g(25℃) | 熔点/℃ | 沸点/℃ |
| X | 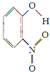 |
0.2 | 45 | 100 |
| Y | 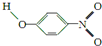 |
1.7 | 114 | 295 |
 价电子(最外层电子)数和重原子(即比氢重的原子)数相同的分子(或离子)互称等电子体.等电子体的结构相似、物理性质相近,称为等电子原理.如N2和CO为等电子体,下表为部分元素等电子体的分类和空间构型表:
价电子(最外层电子)数和重原子(即比氢重的原子)数相同的分子(或离子)互称等电子体.等电子体的结构相似、物理性质相近,称为等电子原理.如N2和CO为等电子体,下表为部分元素等电子体的分类和空间构型表:| 等电子体类型 | 代表物质 | 空间构型 |
| 四原子24电子等电子体 | SO3 | 平面三角形 |
| 四原子26电子等电子体 | SO32- | 三角锥形 |
| 五原子32电子等电子体 | CCl4 | 四面体形 |
| 六原子40电子等电子体 | PCl5 | 三角双锥 |
| 七原子48电子等电子体 | SF6 | 八面体形 |
 根据上述信息,回答下列问题:
根据上述信息,回答下列问题:(1)写出分子或离子的空间构型:IO3-
(2)由第一、二周期元素组成,与氧化性最强的单质分子互为等电子体的分子有N2H4
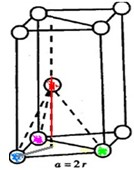
(3)如图是六方最密堆积(Be、Mg、Zn)的晶胞图之一,如果金属镁的密度是ρ g/cm3,且假设镁原子是互相接触的刚性小球,
镁的相对原子质量为M,阿伏加德罗常数为NA,则镁原子的半径为
下列有关物质性质、结构的表述均正确,且存在因果关系的是( )
| 表述Ⅰ | 表述Ⅱ | |
| A | 相同条件下,CO在水中的溶解度比N2大 | 虽然CO与N2互为等电子体,但CO是极性分子,而N2为非极性分子 |
| B | 通常条件下,HF分子比HI分子稳定性高 | HF分子间存在氢键作用,而HI分子间只存在范德华力 |
| C | 在形成化合物时,同一主族元素的化合价相同 | 同一主族元素原子的最外层电子数相同 |
| D | 乙醇、葡萄糖溶于水后均不导电 | 乙醇、葡萄糖均属于共价化合物 |
| A、相同条件下,CO在水中的溶解度比N2大;虽然CO与N2互为等电子体,但CO是极性分子,而N2为非极性分子 |
| B、通常条件下,HF分子比HI分子稳定性高;HF分子间存在氢键作用,而HI分子间只存在范德华力 |
| C、在形成化合物时,同一主族元素的化合价相同;同一主族元素原子的最外层电子数相同 |
| D、乙醇、葡萄糖溶于水后均不导电;乙醇、葡萄糖均属于共价化合物 |
下列物质属于等电子体的一组是( )
| A、CH4和NH3 | B、B3H6N3和C6H6 | C、F-和Mg | D、H2O和CH4 |
下列说法中正确的是( )
| A、SO2和O3、PO43-和C1O4-互为等电子体 | B、甲烷分子失去一个H+,形成CH3-,其碳原子的杂化类型发生了改变 | C、CH4、BCl3、SO2都是含有极性键的非极性分子 | D、所有元素的基态原子核外电子排布都遵循构造原理 |