若某共价化合物分子中只含有C、N、H三种元素,且以n(C)、n(N)分别表示C、N的原子数目,则H原子数目最多等于( )
| A、2n(C)+2+n(N) | B、2n(C)+2+2n(N) | C、2n(C)+2 | D、2n(C)+1+2n(N) |
某天然油脂10.0g,需1.8gNaOH才能使之完全水解;又知1000.0g该油脂硬化加氢时需氢气12.0g,则1mol该油脂中平均含碳碳双键( )
| A、3mol | B、4mol | C、5mol | D、6mol |
碘值是指100g油脂中所能吸收(加成)碘的克数.测得某植物油碘值为a g,以NA表示阿伏加德罗常数,则b g该植物油中含有的碳碳双键数为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
已知含氧酸可用通式XOm(OH)n来表示,如X是S,则m=2,n=2,则这个式子就表示H2SO4.一般而言,该式中m大酸性强,m小的酸性弱.下列各含氧酸中酸性最强的是( )
| A、HClO4 | B、H2SeO3 | C、H3BO3 | D、H3PO4 |
W、X、Y、Z四种元素原子序数依次减小.已知W的原子序数为29;X原子p轨道共有11个电子;Y是第三周期主族元素,其部分电离能数据如下表;Z原子价电子排布式为nsnnpn.请回答下列问题:
(1)W基态原子的电子排布式为 .
(2)电负性:X Y(填“>”、“=”或“<”).
(3)R是与X同主族的短周期元素.R的氢化物沸点比X的氢化物高,原因是 .
(4)Z2X4中,Z原子采用 杂化,每个分子中含有 个σ键, 个π键.
(5)已知W2+能与氨分子形成配离子[W(NH3)4]2+,该配离子中存在的化学键有 .(填标号)
A.金属键 B.离子键 C.共价键 D.配位键.
0 60504 60512 60518 60522 60528 60530 60534 60540 60542 60548 60554 60558 60560 60564 60570 60572 60578 60582 60584 60588 60590 60594 60596 60598 60599 60600 60602 60603 60604 60606 60608 60612 60614 60618 60620 60624 60630 60632 60638 60642 60644 60648 60654 60660 60662 60668 60672 60674 60680 60684 60690 60698 203614
| 电离能/(kJ?mol-1) | I1 | I2 | I3 | I4 | I5 |
| Y | 584 | 1823 | 2751 | 11584 | 14837 |
(2)电负性:X
(3)R是与X同主族的短周期元素.R的氢化物沸点比X的氢化物高,原因是
(4)Z2X4中,Z原子采用
(5)已知W2+能与氨分子形成配离子[W(NH3)4]2+,该配离子中存在的化学键有
A.金属键 B.离子键 C.共价键 D.配位键.
 (1)依据第2周期元素第一电离能的变化规律,参照如图中B、F元素的位置,用小黑点标出C、N、O三种元素的相对位置.
(1)依据第2周期元素第一电离能的变化规律,参照如图中B、F元素的位置,用小黑点标出C、N、O三种元素的相对位置.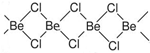 锂和铍单质及化合物的性质具有特殊性.
锂和铍单质及化合物的性质具有特殊性.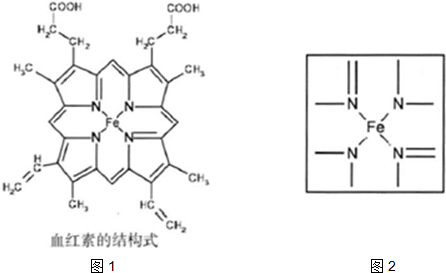
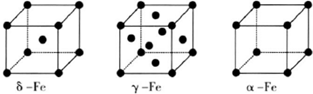
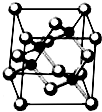 Ⅰ.砷化镓为第三代半导体,以其为材料制造的灯泡寿命长.耗能少.已知砷化镓的晶胞结构如图所示.请回答下列问题:
Ⅰ.砷化镓为第三代半导体,以其为材料制造的灯泡寿命长.耗能少.已知砷化镓的晶胞结构如图所示.请回答下列问题: